Für viele in unserer Gemeinschaft beginnt die Reise mit synovialem Sarkom nicht mit Klarheit, sondern mit einer frustrierenden und oft langen Suche nach Antworten.[1] Wir wissen, dass dieser Weg oft mit Ungewissheit gepflastert ist. Da es sich um eine seltene Krebserkrankung handelt, die hauptsächlich Jugendliche und junge Erwachsene (die AYA-Population) betrifft, werden die anfänglichen Symptome – oft ein schmerzloser, langsam wachsender Knoten – häufig mit etwas Gewöhnlichem, wie einer Sportverletzung oder einer Zyste, verwechselt.[2][4] Dies kann zu einer "diagnostischen Odyssee" führen, die bis zu zwei Jahre dauern kann, eine kritische Verzögerung für einen aggressiven Krebs.[1]
Diese Diagnose trifft junge Menschen zu einem entscheidenden Zeitpunkt in ihrem Leben, unterbricht die Ausbildung, Karrieren und Familienplanung. Seit Jahrzehnten war der Weg für diejenigen mit fortgeschrittenen oder metastasierten Erkrankungen einschüchternd. Standard-Chemotherapie-Regime haben, obwohl wichtig, nur begrenzten langfristigen Erfolg geboten.[3] Für Erwachsene mit metastasiertem synovialem Sarkom lag die fünfjährige Gesamtüberlebensrate bei düsteren 10%.[3] Zweitlinientherapien wie Pazopanib oder Trabectedin, während sie Optionen bieten, gewähren typischerweise bescheidene Vorteile, wobei das mediane Gesamtüberleben bei etwa 10 Monaten schwebt.[5] Es gab ein tiefes, spürbares unerfülltes Bedürfnis nach einem echten Durchbruch.
Aber heute möchten wir Sie durch eine Geschichte des wissenschaftlichen Fortschritts führen, die eine neue Art von Hoffnung bietet. Es handelt sich um eine Therapie, die nicht nur den Krebs bekämpft, sondern dem eigenen Körper des Patienten beibringt, wie man es tut. Wir sprechen von einer wegweisenden neuen Behandlung namens Afamitresgene Autoleucel oder Tecelra.[11]
Dies ist eine tiefe Eintauchung in die Wissenschaft, die Hoffnung und die realistischen Herausforderungen dieses neuen Frontiers. Wir glauben, dass wir durch das Verständnis mehr informierte Gespräche mit unseren Betreuungsteams führen, bessere Fragen stellen und gemeinsam mit einem klareren Gefühl dessen, was die Zukunft bringen könnte, voranschreiten können. Diese Therapie ist nicht nur ein neues Medikament; es ist ein neues Kapitel, das den Kern dessen erreicht, was synoviales Sarkom einzigartig macht.
Die Wissenschaft: Ein Schloss, ein Schlüssel und ein ausgebildeter Soldat
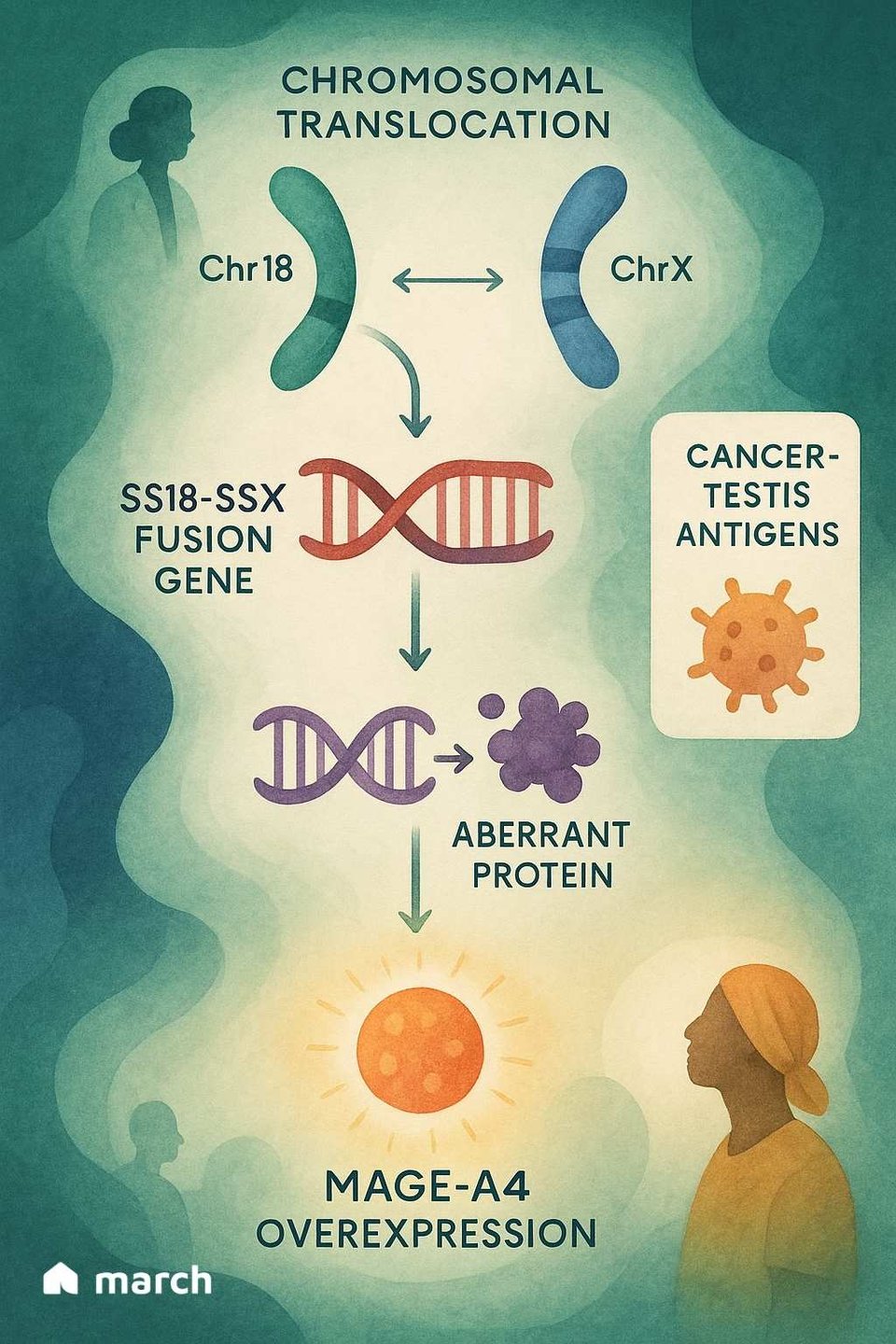
Um die Bedeutung von Tecelra wirklich zu begreifen, müssen wir mit der einzigartigen Biologie des synovialen Sarkoms selbst beginnen. Anders als viele Krebsarten, die Hunderte von verschiedenen genetischen Mutationen aufweisen, ist das synoviale Sarkom oft "mutational ruhig".[4] Über 95% der Fälle werden durch ein einzelnes, spezifisches genetisches Ereignis getrieben: eine Translokation, bei der Teile von Chromosom 18 und Chromosom X ihre Plätze tauschen.[6][7] Dies schafft ein kraftvolles und zerstörerisches Fusionsgen namens SS18-SSX.[6]
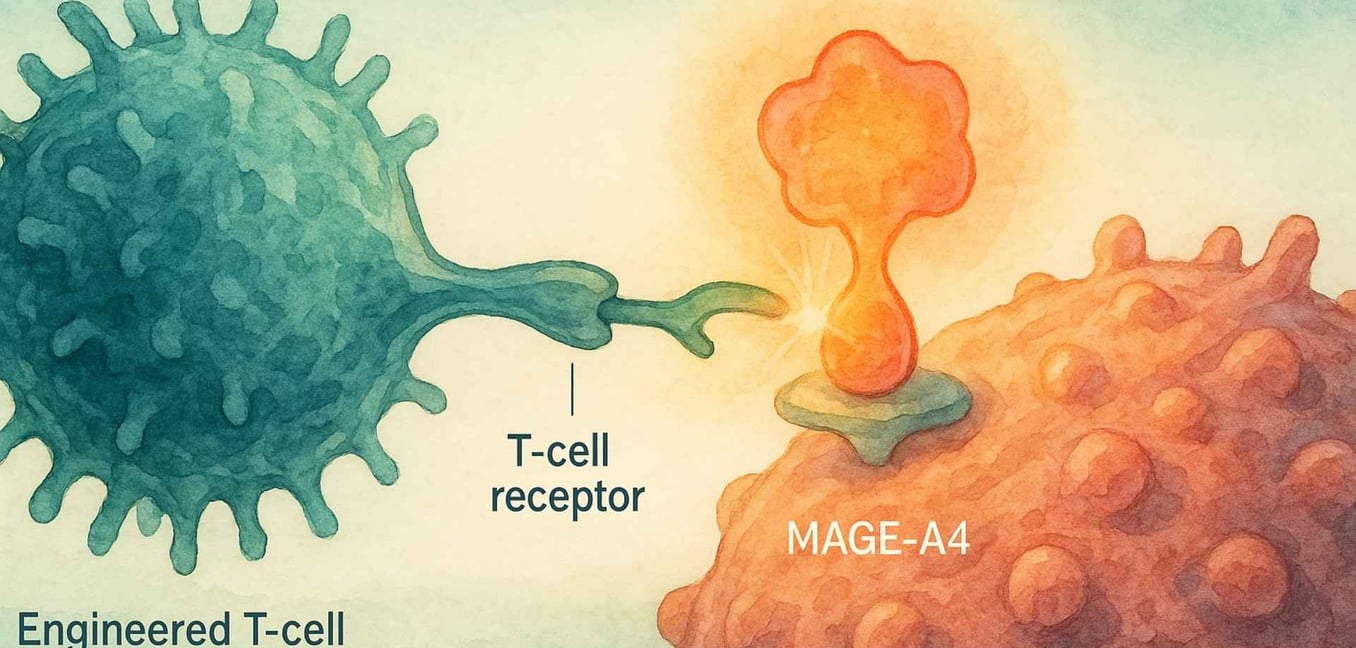
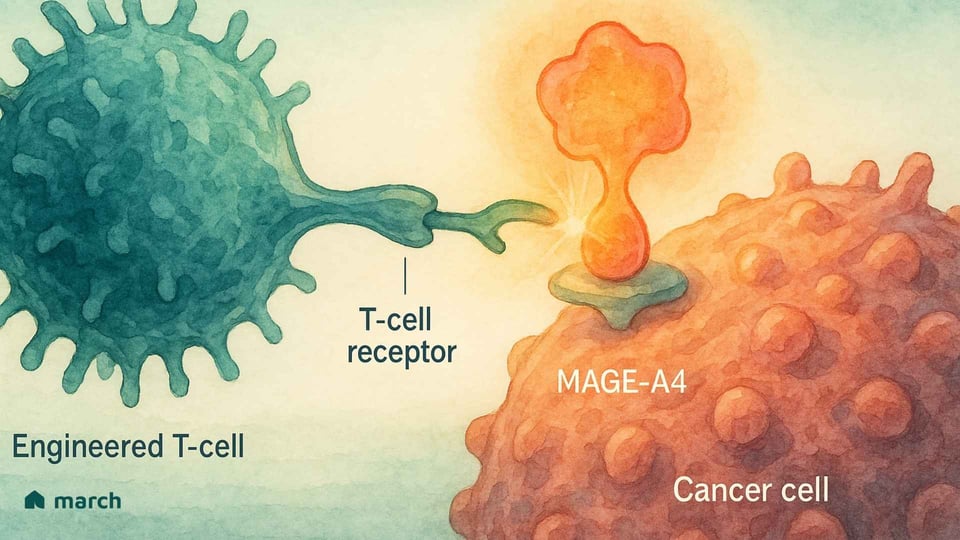
Dieses SS18-SSX-Fusionsprotein verursacht nicht allein Krebs; stattdessen kapert es die innere Maschinerie der Zelle, die steuert, welche Gene aktiviert oder deaktiviert werden.[6] Eine der Konsequenzen dieses genetischen Chaos ist, dass die Krebszellen Proteine produzieren, die normale adulte Zellen nicht produzieren, darunter ein Protein namens MAGE-A4.[8]
MAGE-A4 ist ein "Krebs-Hoden-Antigen", was bedeutet, dass es normalerweise nur an immunprivilegierten Orten wie den Hoden gefunden wird.[9] Wenn es auf einer Sarkomazelle erscheint, wirkt es wie eine fremde Flagge und signalisiert dem Immunsystem, dass etwas nicht stimmt.[8] Hier kommt die elegante Strategie von Tecelra ins Spiel.
Von CAR-T zu TCR: Zielen auf das Unberührbare
Viele von uns haben von CAR-T-Therapie gehört, die revolutionär für Blutkrebserkrankungen war.[10] CAR-T-Zellen werden so entwickelt, dass sie Zielstrukturen auf der Oberfläche von Krebszellen erkennen. Allerdings sind die meisten krebsverursachenden Proteine, wie MAGE-A4, innerhalb der Zelle verborgen, was sie für CAR-T unsichtbar macht.[20]
Hier kommt T-Zell-Rezeptor (TCR)-Therapie ins Spiel. Alle unsere Zellen verwenden ein System namens HLA-Komplex, um kontinuierlich dem Immunsystem Stücke der Proteine in ihrem Inneren zu zeigen.[13] Wenn eine Zelle krebsartig ist, zeigt sie Fragmente von Krebsproteinen an ihrer Oberfläche. TCR-T-Zell-Therapie entwickelt die T-Zellen eines Patienten so, dass sie diese sehr spezifischen Fragmente erkennen.[20]
Tecelra ist die erste von der FDA zugelassene TCR-Therapie für einen soliden Tumor, ein wahrhaft wegweisender Meilenstein.[11] Es funktioniert, weil es zwei Probleme gleichzeitig löst:
Das Schloss (Das Ziel): Es gibt den T-Zellen eines Patienten einen neuen, hochaffinen TCR, der fachgerecht entworfen wurde, um das MAGE-A4-Proteinstück zu finden.[13]
Der Schlüssel (Der Handschlag): Es kann dieses Fragment nur "sehen", wenn es von einem bestimmten HLA-Molekül, HLA-A*02, präsentiert wird.[13]
Dieses zweigeteilte Erkennungssystem – das MAGE-A4 "Schloss" und der HLA-A*02 "Schlüssel" – macht die Therapie unglaublich präzise, aber auch hochgradig personalisiert.[13] Es wird nur für Patienten funktionieren, die beide biologischen Marker haben.[14]
Der Tecelra-Prozess: Die Reise eines Patienten zu einer Lebenden Medizin
Die Wissenschaft zu verstehen, ist eine Sache; zu wissen, was die Reise tatsächlich beinhaltet, eine andere. Der Prozess, Tecelra zu erhalten, ist intensiv und erfordert von Patienten und ihren Betreuern ein erhebliches Engagement. Es ist ein mehrstufiger Weg, der die eigenen Zellen eines Patienten in eine kraftvolle, lebende Medizin verwandelt.
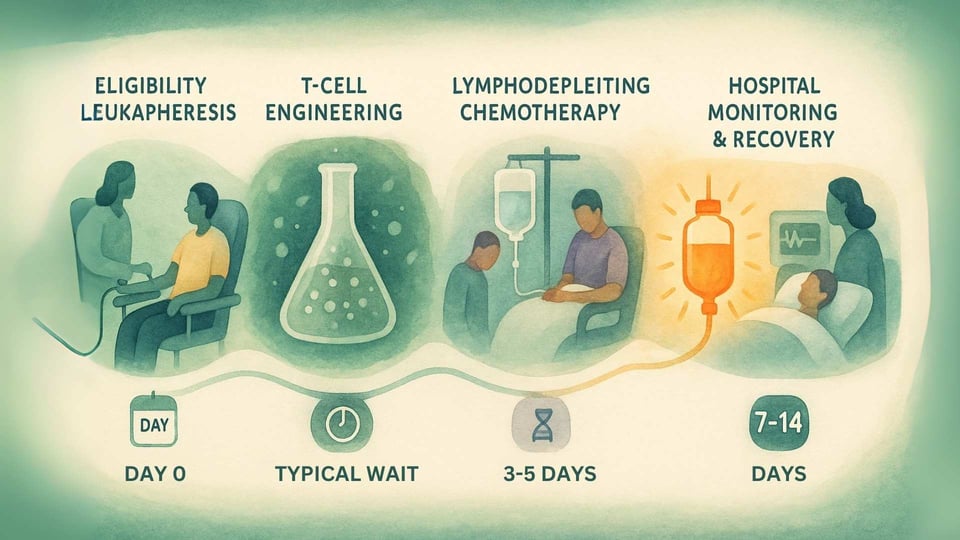
Schritt 1: Bestätigung und Sammlung (Leukapherese)
Die Reise beginnt mit Tests, um sicherzustellen, dass ein Patient geeignet ist. Dazu gehört ein Bluttest, um zu bestätigen, dass er den erforderlichen HLA-A*02 genetischen Marker hat, und ein Biopsietest seines Tumors, um zu bestätigen, dass er das MAGE-A4-Protein exprimiert.[14] Nach Bestätigung der Eignung unterzieht sich der Patient einer Leukapherese, einem nicht-chirurgischen Verfahren, das T-Zellen aus seinem Blut filtert.[12]
Schritt 2: Die Herstellungswartezeit
Die gesammelten T-Zellen werden eingefroren und an eine spezialisierte Produktionsstätte geschickt. Dort durchlaufen sie den genetischen Ingenieurierungsprozess, um zu Tecelra zu werden.[13] Dies ist ein komplexer und sorgfältiger Prozess, der in der klinischen Studie im Median 40 Tage dauerte.[14] Während dieser Wartezeit kann der Arzt des Patienten eine "Überbrückungstherapie" wie Chemotherapie empfehlen, um den Krebs unter Kontrolle zu halten.[14]
Schritt 3: Den Körper vorbereiten (Lymphodepletion)
Einige Tage vor der Infusion wird der Patient ins Krankenhaus eingeliefert, um eine lymphodepletierende Chemotherapie zu erhalten (typischerweise Fludarabin und Cyclophosphamid).[14] Das Ziel dieser Chemotherapie ist es nicht, den Krebs zu töten, sondern vorübergehend die Anzahl der vorhandenen Immunzellen im Körper zu reduzieren.[15] Dies schafft eine klare und einladende Umgebung für die neuen, entwickelten T-Zellen, um sich anzusiedeln, zu wachsen und eine langfristige Wirkung zu erzielen.[15]
Schritt 4: Die Infusion (Tag Null)
Nach der Lymphodepletion erhält der Patient seine personalisierten Tecelra-Zellen durch eine einzelne intravenöse (IV) Infusion.[14] Dieser Moment wird oft als "Tag Null" bezeichnet und kennzeichnet den Beginn des Kampfes seines neuen Immunsystems gegen den Krebs.
Schritt 5: Intensive Überwachung und Unterstützung
Die Zeit nach der Infusion ist die kritischste. Da die Therapie darauf ausgelegt ist, eine starke Immunreaktion zu erzeugen, müssen die Patienten im Krankenhaus für mindestens 7 Tage überwacht werden.[14] Sie werden außerdem geraten, mindestens 4 Wochen in der Nähe des spezialisierten Behandlungszentrums zu bleiben. Die Hersteller bieten ein Unterstützungsprogramm, AdaptimmuneAssist, das berechtigten Patienten bei Reise-, Unterkunfts- und anderen aus eigener Tasche zu zahlenden Kosten helfen kann.[16]
Eine Geschichte, die in Daten erzählt wird: Die Hoffnung der SPEARHEAD-1-Studie
Jahrelang war diese bemerkenswerte Wissenschaft ein Konzept, das in Laboren erforscht wurde. Aber die SPEARHEAD-1 klinische Studie brachte sie von der Theorie in die Realität und bot 44 Menschen mit fortgeschrittenem synovialem Sarkom, die bereits eine mediane Anzahl von drei vorangegangenen systemischen Therapien durchlaufen hatten, greifbare Hoffnung.[14][17] Dies waren Patienten, bei denen die Standardoptionen nicht mehr funktionierten. Die Ergebnisse, veröffentlicht in der angesehenen Zeitschrift The Lancet, waren eine Quelle unglaublicher Ermutigung.[14]
Lassen Sie uns die Zahlen betrachten, denn sie erzählen eine kraftvolle Geschichte der Hoffnung:
Eine signifikante Reaktion (ORR): In dieser stark vorbehandelten Gruppe sahen 43% der Patienten, dass sich ihre Tumore als Reaktion auf die einmalige Infusion von Tecelra verkleinerten.[11][14] Dies wird als Gesamtansprechrate (ORR) bezeichnet, und es ist eine signifikante Zahl, bei der spätere Therapien oft Ansprechraten von weit unter 20% haben.
Langlebige, dauerhafte Vorteile (DoR): Für diejenigen, die auf die Therapie angesprochen haben, waren die Wirkungen oft dauerhaft. Die mediane Antwortdauer (DoR) betrug 6,0 Monate.[14] Entscheidend ist, dass 39% derjenigen, die angesprochen haben, diesen Nutzen auch ein Jahr später noch sahen, was auf einen langlebigen, langfristigen Effekt für eine signifikante Gruppe hindeutet.[14]
Das "Schwänzchen auf der Kurve" (Gesamtüberleben): Vielleicht die eindrucksvollste Erkenntnis war, was mit den Patienten geschah, die auf Tecelra langfristig ansprachen. Für die gesamte Gruppe von Patienten mit synovalem Sarkom lag das mediane Gesamtüberleben (OS) bei etwa 17 Monaten.[14] Aber für diejenigen, deren Krebs auf die Therapie ansprach, war das mediane OS noch nicht erreicht, und schätzungsweise 70% dieser Ansprechenden waren zum zweijährigen Zeitpunkt noch am Leben.[14] Dies schafft, was Forscher als "Schwänzchen auf der Überlebenskurve" bezeichnen. Es deutet darauf hin, dass für eine Teilmenge von Patienten diese lebende Medizin nicht nur eine vorübergehende Lösung ist; sie hat das Potenzial, einen langfristigen, dauerhaften Schutz gegen den Krebs zu bieten und somit ihre Perspektive grundlegend zu verändern.
Für eine Gemeinschaft, die über ein Jahrzehnt auf eine neue therapeutische Option gewartet hat, stellen diese Ergebnisse einen monumentalen und emotionalen Fortschritt dar. Es ist derartige Fortschritte, die zeigen, dass die Wissenschaft hört und dass die Bedürfnisse der Patienten mit seltenen Erkrankungen Innovationen vorantreiben.
Der Weg nach vorne: Realismus, Verantwortung und der Horizont
Wir gehen diesen Weg mit Ihnen, halten sowohl Hoffnung als auch Ehrlichkeit. Dies ist eine kraftvolle Therapie, und es ist wichtig, die erheblichen Nebenwirkungen zu verstehen. Da es darauf abzielt, das Immunsystem stark zu aktivieren, kommt Tecelra mit einer US-Boxed Warning für zwei Haupttoxizitäten, die potenziell lebensbedrohlich sind:[11]
Zytokinfreisetzungssyndrom (CRS): Dies war die häufigste schwere Nebenwirkung, die bei 75% der Patienten in der Studie auftrat.[14] CRS ist eine systemische Entzündungsreaktion, die hohes Fieber, Übelkeit, niedrigen Blutdruck und andere Symptome verursachen kann. Während die meisten Fälle mild bis moderat sind und effektiv mit unterstützender Pflege und Medikamenten behandelt werden können, erlebten 2% der Patienten schwere (Grad 3 oder höher) CRS.[14]
Neurotoxizitätssyndrom, das mit immunaktiven Zellen assoziiert ist (ICANS): Dies ist eine seltenere neurologische Nebenwirkung, die bei etwa 2% der Patienten in geringem Maße zu beobachten war.[14]
Diese Risiken sind genau der Grund, warum Tecelra nur in spezialisierten, autorisierten Behandlungszentren mit fachkundig geschulten Teams verabreicht werden kann.[18]
Die Ankunft von Tecelra ist wirklich eine neue Dämmerung, aber wir wissen, dass es nicht das Ende der Reise ist. Die Diskussion über fortschrittliche Therapien muss die Herausforderungen des Zugangs und der Kosten einschließen. Mit einem angegebenen Listenpreis von 727.000 USD ist die Gewährleistung eines gerechten Zugangs eine große ethische und praktische Herausforderung für unser Gesundheitssystem.[19] Als Befürworter müssen wir weiterhin auf eine Zukunft drängen, in der jeder Berechtigte profitieren kann.
Die Geschichte von Tecelra handelt von mehr als nur einem einzelnen Medikament. Es geht um den unermüdlichen Fortschritt der Wissenschaft, und es öffnet die Tür zu künftiger Innovation. Die Forschung ist bereits im Gange, die anderen Ziele wie das NY-ESO-1-Antigen und nächste Generation TCRs, die noch effektiver sein sollen, zu untersuchen.[20]
Während wir diese neue Frontlinie beobachten, sind wir verpflichtet, Ihnen klare, vertrauenswürdige Informationen bereitzustellen. Ihre Einsichten, Ihre Erfahrungen und Ihre Hoffnung sind es, die diesen Fortschritt antreiben. Auf dieser Entdeckungsreise sind Sie nicht allein.
Quellen
Aytekin, M. N., et al. (2022). Der "Große Maskenbildner" in der Orthopädie: Synoviales Sarkom. Cureus.
Orphanet. (n.d.). Synoviales Sarkom.
National Cancer Institute. (n.d.). Behandlung des synovialen Sarkoms (PDQ®) – Version für Gesundheitsfachkräfte.
King, D.M., et al. (2020). Eine Übersicht über synoviales Sarkom. Journal of the American Academy of Orthopaedic Surgeons.
Martin-Broto, J., et al. (2022). Pazopanib und Trabectedin für Patienten mit metastasiertem synovialem Sarkom: Eine realweltliche Studie. Cancers.
Lagarde, P., et al. (2016). Das SS18-SSX Fusions-Onkoprotein. The Journal of Pathology.
PathologyOutlines.com. (n.d.). Synoviales Sarkom - Molekular.
Saito, T., et al. (2023). MAGE-A4 ist ein potenzielles therapeutisches Ziel im synovialen Sarkom. Oncology Reports.
Cancer Research Institute. (n.d.). Krebs-Hoden-Antigene.
National Cancer Institute. (n.d.). CAR-T-Zelltherapie und deren Nebenwirkungen.
U.S. Food and Drug Administration. (2024). FDA gewährt beschleunigte Genehmigung für Afamitresgene Autoleucel.
National Cancer Institute. (n.d.). Leukapherese. NCI-Wörterbuch der Krebsterme.
Adaptimmune. (n.d.). Unsere Technologie.
D'Angelo, S. P., et al. (2024). Afamitresgene Autoleucel für fortgeschrittenes synoviales Sarkom (SPEARHEAD-1). The Lancet.
Jain, T., et al. (2019). CAR-T-Zelltherapie: Die Rolle der Lymphodepletion. The Hematologist.
Adaptimmune. (n.d.). AdaptimmuneAssist.
D'Angelo, S. P., et al. (2021). Afamitresgene Autoleucel für fortgeschrittenes synoviales Sarkom oder myxoides/rundzelliges Liposarkom. ASCO Post.
Adaptimmune. (n.d.). Autorisierte Behandlungszentren.
Leo, L. & Sunny, S.E. (2024). US FDA genehmigt Adaptimmunes Gentherapie für seltenen Krebs. Reuters.
Ma, S., et al. (2021). Aktuelle Landschaft der T-Zell-Rezeptor-engineerten T-Zell-Therapie für solide Tumoren. Journal of Hematology & Oncology.