
Für so viele Familien in unserer Gemeinschaft beginnt die Reise mit einer ultrararen Krankheit oft mit einem Fragezeichen. Es ist ein Weg, der oft eine lange, frustrierende Suche nach Antworten beinhaltet – eine "diagnostische Odyssee" – und zu einem Leben führt, in dem komplexe Symptome ohne eine Therapie, die das Grundproblem angeht, verwaltet werden müssen. Wir wissen, dass diese Reise unglaublich herausfordernd sein kann, und wir möchten, dass Sie wissen, dass Sie auf diesem Weg nicht allein sind.
Heute möchten wir Sie durch eine Geschichte des unglaublichen wissenschaftlichen Fortschritts führen, die ein neues Kapitel der Hoffnung für eine solche Erkrankung bringt: das WHIM-Syndrom.
Dies ist ein tiefgehender Einblick in die Wissenschaft, die Herausforderungen und den bahnbrechenden Fortschritt, der zur ersten Therapie geführt hat, die speziell für diese seltene Erkrankung entwickelt wurde. Wir glauben, dass wir durch das Verständnis der Reise von der Entdeckung zur Behandlung informiertere Gespräche führen, bessere Fragen stellen und gemeinsam mit einem klareren Gefühl dafür, was die Zukunft für unsere Gemeinschaften bereithält, vorankommen können.
Was ist das WHIM-Syndrom? Eine Geschichte in einem Akronym
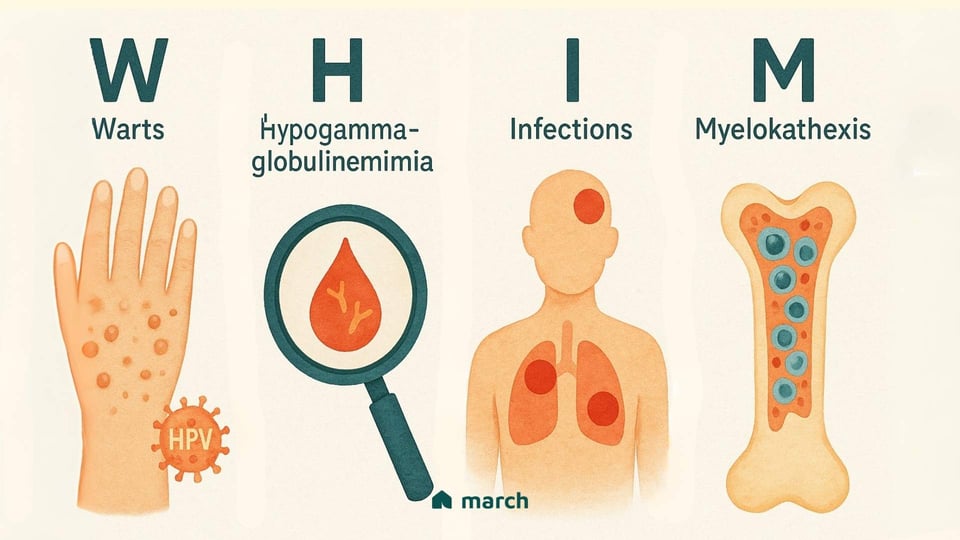
Das WHIM-Syndrom ist eine extrem seltene, genetische primäre Immunodefizienz, und sein Name ist ein Akronym, das die Geschichte seiner Hauptmerkmale erzählt:[1]
Warzen: Patienten erleben oft schwere, anhaltende und weit verbreitete Warzen, die durch eine ungewöhnliche Anfälligkeit für das Humane Papillomavirus (HPV) verursacht werden.
Hypogammaglobulinämie: Dies bedeutet, dass niedrige Werte von Immunglobulinen (Antikörpern) im Blut vorhanden sind, die die wesentlichen Werkzeuge des Körpers zum Bekämpfen von Bakterien und anderen Keimen sind.
Infektionen: Die Kombination der Herausforderungen des Immunsystems führt zu wiederkehrenden und oft schwerwiegenden bakteriellen Infektionen, wie Pneumonie, Sinusitis und Hautinfektionen.
Myelokathexis: Dies ist der wissenschaftliche Begriff für das ungewöhnliche und prägende Merkmal von WHIM. Es beschreibt eine Situation, in der die Schlüsselzellen des Körpers zur Bekämpfung von Infektionen, insbesondere Neutrophile, im Knochenmark "gefangen" sind und nicht in den Blutkreislauf gelangen können, um ihre Arbeit zu tun.[2]
Stellen Sie sich vor, die besten Soldaten Ihres Körpers sind alle ausgebildet und bereit für den Kampf, aber sie sind hinter einer verriegelten Tür in der Kaserne festgehalten, unfähig, an die Front zu gelangen.[3] Dies ist das Kernproblem des WHIM-Syndroms. Das Knochenmark ist voll von gesunden, reifen Immunzellen, aber der Rest des Körpers bleibt anfällig.
Die Wurzel des Problems: Eine überaktive "Türglocke" im Immunsystem
Was hält also diese Tür verriegelt? Jahrzehntelang war das ein Rätsel. Doch 2003 machten Forscher einen bahnbrechenden Entdeckung: Das WHIM-Syndrom wird verursacht durch eine Mutation in einem Einzelgen namens CXCR4.[4]
Dieses Gen liefert die Anweisungen für einen Rezeptor, der wie eine zelluläre "Türglocke" funktioniert. Er befindet sich an der Oberfläche von weißen Blutkörperchen und seine Hauptaufgabe ist es, ein Signal von einem Molekül namens CXCL12 zu empfangen. Dieses Signal sagt im Wesentlichen den weißen Blutkörperchen, dass sie im sicheren, nährenden Umfeld des Knochenmarks bleiben sollen.[5]
Bei einer gesunden Person klingelt diese Türglocke, die Zelle erhält die "bleib hier"-Nachricht, und dann wird die Türglocke schnell abgeschaltet. Dies ermöglicht es den Zellen, das Knochenmark zu verlassen, wenn sie gerufen werden, um eine Infektion zu bekämpfen.
Im Fall des WHIM-Syndroms bewirkt die Mutation eine “Funktionsgewinn.” Das bedeutet, dass die CXCR4-Türglocke überaktiv ist – sie ist im Grunde im "eingeschaltet"-Zustand festgefahren.[6] Sie sendet ständig das Signal, dass die Zellen bleiben sollen, selbst wenn es kein aktives Signal gibt, das es ihnen sagt.
Dies ist die direkte Ursache der Myelokathexis. Das unaufhörliche "bleib hier"-Signal des defekten CXCR4-Rezeptors ist es, was die Tür verriegelt und reife Neutrophile und Lymphozyten im Knochenmark gefangen hält. Dort werden sie schließlich alt und sterben, ohne jemals die Teile des Körpers zu erreichen, die sie dringend benötigen. Dieser einzige genetische Tippfehler führt zu den niedrigen weißen Blutkörperchen (Neutropenie und Lymphopenie), die die wiederholten Infektionen und anderen Symptome des WHIM verursachen.
Die Reise zu einer Lösung: Vom Verwalten der Symptome zum Anvisieren der Ursache
Über Jahrzehnte hinweg bedeutete das Management des WHIM-Syndroms, die Konsequenzen der verriegelten Tür zu behandeln, nicht das Schloss selbst. Diese unterstützende Pflege war und bleibt eine wichtige Lebenslinie für Patienten.
Granulozyten-Kolonie-stimulierender Faktor (G-CSF) Injektionen können helfen, mehr Neutrophile aus dem Knochenmark zu drängen, aber diese Behandlung adressiert nicht das zugrunde liegende Problem mit anderen Immunzellen und kann langfristige Risiken mit sich bringen.[1]
Immunoglobulin (IVIG) Infusionen können dem Körper geliehene Antikörper zur Bekämpfung von Infektionen bereitstellen, aber das ist eine temporäre Lösung, die lebenslange, belastende Infusionen erfordert.
Dies sind unglaublich wichtige Werkzeuge, aber sie sind "Umgehungen." Sie beheben die defekte Türglocke nicht. Die Gemeinschaft hat schon lange eine Therapie benötigt, die die genetische Ursache der Krankheit direkt ansprechen kann.
Ein bahnbrechender Moment: Das Eintreffen von Mavorixafor (XOLREMDI®)
Nach Jahren engagierter Forschung kam ein bahnbrechender Moment. Im April 2024 genehmigte die U.S. FDA mavorixafor (Markenname XOLREMDI®), die erste und einzige Therapie, die speziell zur gezielten Bekämpfung des zugrunde liegenden Mechanismus des WHIM-Syndroms entwickelt wurde für Patienten ab 12 Jahren.[7]
Kehren wir zu unserer Analogie zurück. Wenn das Problem eine überaktive Türglocke ist, funktioniert Mavorixafor, indem es vorübergehend eine Abdeckung darüber legt.
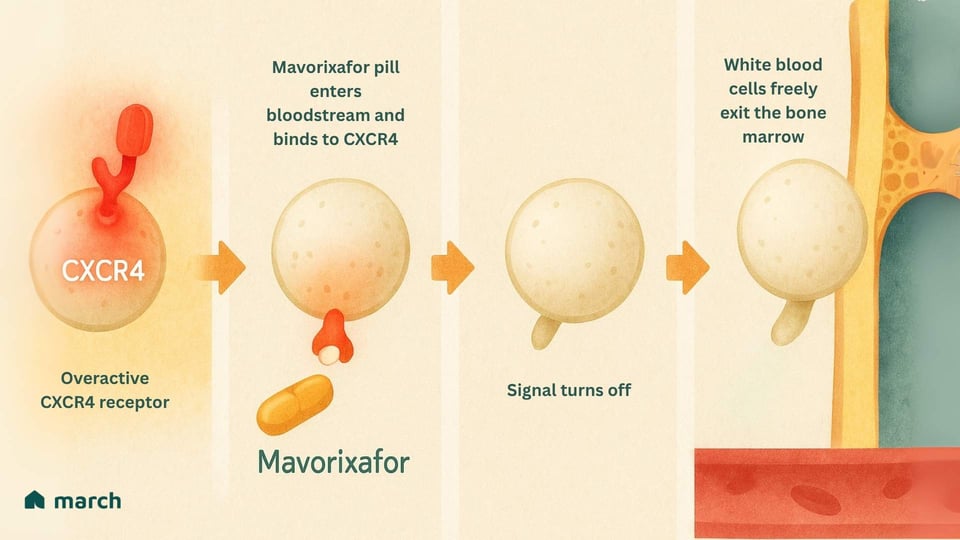
Mavorixafor ist ein orales Medikament, das ein CXCR4-Antagonist ist. Das bedeutet, dass es an den CXCR4-Rezeptor bindet und ihn blockiert, wodurch verhindert wird, dass er ständig sein "bleib hier"-Signal sendet.[8]
Durch das Unterbrechen dieses Signals "öffnet es die Tür." Die gefangenen Neutrophile und Lymphozyten werden schließlich aus dem Knochenmark freigesetzt und können in den Blutkreislauf gelangen, um nach Infektionen zu patrouillieren und den Körper zu schützen.[7]
Die Ergebnisse aus der entscheidenden Phase-3-Studie waren eine Quelle tiefgreifender Hoffnung für die Gemeinschaft. Patienten, die Mavorixafor einnahmen, sahen:[9]
Ein statistisch signifikanter Anstieg der Zeit, in der ihre Neutrophil- und Lymphozyt-Werte über den Niveaus lagen, die benötigt werden, um Infektionen zu bekämpfen.
Am stärksten war eine 60%ige Verringerung der Rate schwerer Infektionen im Vergleich zu denen, die ein Placebo erhielten.
Dies stellt einen monumentalen Schritt nach vorn dar – einen Wechsel von der bloßen Behandlung der Folgen der Krankheit hin zur aktiven Intervention an der Quelle.
Gemeinsam vorankommen: Hoffnung, Realismus und die bevorstehende Reise
Die Genehmigung einer gezielten Therapie für eine ultrarare Krankheit ist ein Sieg für die gesamte Gemeinschaft seltener Erkrankungen. Es ist ein Zeugnis für die Widerstandsfähigkeit der Patienten und Familien, die an klinischen Studien teilnehmen, und für die Hingabe der Forscher und Befürworter, die den Fortschritt unterstützen.
Gleichzeitig gehen wir als Gemeinschaft diesen Weg mit Hoffnung und Ehrlichkeit. Dies ist ein großer Schritt, aber es ist nicht das Ende der Reise. In der Hauptstudie zeigte die Therapie keinen signifikanten Fortschritt in der Belastung durch Warzen, und ihre Genehmigung gilt derzeit für Patienten ab 12 Jahren, was einen anhaltenden Forschungsbedarf bei jüngeren Kindern unterstreicht.[9,10] Mavorixafor ist eine tägliche, lebenslange Managementtherapie, kein einmaliges Heilmittel, und erfordert sorgfältige Befolgung.
So sieht der Fortschritt aus. Es ist ein engagierter, bedeutungsvoller Schritt, der die Belastung durch Infektionen erheblich verringern und die Art und Weise, wie eine Krankheit behandelt wird, transformieren kann. Und es inspiriert die nächste Welle der Innovation. Die bemerkenswerte Geschichte einer Patientin, die sich spontan vom WHIM erholt hat, als ein genetischer Unfall ihr defektes CXCR4-Gen löschte, hat einen natürlichen Proof-of-Concept für eine mögliche Heilung geliefert und die Forschung nach Gentherapien angestoßen, die eines Tages dieses Ergebnis absichtlich replizieren könnten.[11]
Während wir diese neuen Grenzen der Medizin beobachten, setzen wir uns dafür ein, Ihnen klare, zuverlässige Informationen bereitzustellen. Wir werden die Fortschritte feiern und ehrlich über die verbleibenden Herausforderungen sprechen. Wir werden weiterhin eine Gemeinschaft aufbauen, in der wir lernen, teilen und uns gegenseitig unterstützen können. Ihre Einsichten, Ihre Erfahrungen und Ihre Hoffnung sind das, was diesen vorwärts gerichteten Marsch antreibt. Auf dieser Entdeckungsreise sind Sie nicht allein.
Um einen schnellen Überblick über einen weiteren wissenschaftlichen Durchbruch zu erhalten, hören Sie sich unsere neueste Podcast-Episode an, die die Geschichte und Wissenschaft hinter neuen Genbearbeitungstherapien behandelt.
Quellen
[1] National Organization for Rare Disorders (NORD). (n.d.). WHIM-Syndrom.
[2] Zuelzer, W. W. (1964). "Myelokathexis" – eine neue Form der chronischen Granulozytopenie. New England Journal of Medicine.
[3] Dale, D. C., et al. (2020). Der CXCR4-Antagonist Mavorixafor bei Patienten mit WHIM-Syndrom. Blood.
[4] Hernandez, P. A., et al. (2003). Mutationen im Chemokinrezeptor-Gen CXCR4 sind mit dem WHIM-Syndrom, einer kombinierten Immunedefizienzkrankheit, assoziiert. Nature Genetics.
[5] X4 Pharmaceuticals. (2024). XOLREMDI (Mavorixafor) Verschreibungsinformationen.
[6] Balabanian, K., et al. (2005). WHIM-Syndrome mit unterschiedlichen genetischen Anomalien werden durch beeinträchtigte CXCR4-Desensibilisierung und Internalisierung erklärt. Blood.
[7] Badalato, R., et al. (2024). Mavorixafor zur Behandlung des WHIM-Syndroms: eine Phase-3, randomisierte, placebo-kontrollierte Studie. The Lancet.
[8] McDermott, D. H., et al. (2019). Der CXCR4-Antagonist Plerixafor korrigiert die Panleukopenie und verhindert bakterielle Infektionen beim WHIM-Syndrom. Blood.
[9] X4 Pharmaceuticals. (2024, 29. April). X4 Pharmaceuticals kündigt die Genehmigung durch die U.S. FDA von XOLREMDI™ (Mavorixafor) an. [Pressemitteilung].
[10] U.S. Food & Drug Administration (FDA). (2024). Neuartige Arzneimittelgenehmigungen für 2024.
[11] McDermott, D. H., et al. (2015). Chromothriptische Heilung des WHIM-Syndroms. Cell.










Sadaf boostan
•3 Monate, 4 Wochen her
Großartig
Report Comment
You are about to report:
Sadaf boostan
sadaf sadaf
•3 Monate her
Toll
Report Comment
You are about to report:
sadaf sadaf