Para muchos en nuestra comunidad, el viaje con sarcoma sinovial comienza no con claridad, sino con una búsqueda frustrante y a menudo prolongada de respuestas.[1] Sabemos que este camino a menudo está lleno de incertidumbre. Debido a que es un cáncer raro, que afecta principalmente a adolescentes y adultos jóvenes (la población AYA), sus síntomas iniciales—frecuentemente un bulto indoloro y de crecimiento lento—se confunden a menudo con algo más común, como una lesión deportiva o un quiste.[2][4] Esto puede llevar a una "odisea diagnóstica" que puede durar hasta dos años, un retraso crítico para un cáncer agresivo.[1]
Este diagnóstico recae sobre personas jóvenes en un momento crucial de sus vidas, interrumpiendo la educación, las carreras y la planificación familiar. Durante décadas, el camino a seguir para aquellos con enfermedad avanzada o metastásica ha sido desalentador. Los regímenes de quimioterapia estándar, aunque importantes, han ofrecido un éxito limitado a largo plazo.[3] Para los adultos diagnosticados con sarcoma sinovial metastásico, la tasa de supervivencia general a cinco años ha sido sombría, del 10%.[3] Los tratamientos de segunda línea, como pazopanib o trabectedin, aunque ofrecen opciones, normalmente brindan beneficios modestos, con una supervivencia media general que ronda los 10 meses.[5] Ha habido una profunda y sentida necesidad insatisfecha de un verdadero avance.
Pero hoy, queremos caminar contigo a través de una historia de progreso científico que ofrece un nuevo tipo de esperanza. Es una terapia que no solo combate el cáncer, sino que enseña al propio cuerpo del paciente cómo hacerlo. Hablamos de un nuevo tratamiento pionero llamado afamitresgene autoleucel, o Tecelra.[11]
Esta es una inmersión profunda en la ciencia, la esperanza y los retos realistas de esta nueva frontera. Creemos que al entenderlo, podemos tener conversaciones más informadas con nuestros equipos de atención, hacer mejores preguntas y avanzar juntos con una visión más clara de lo que puede deparar el futuro. Esta terapia no es solo un nuevo fármaco; es un nuevo capítulo, uno que llega al corazón mismo de lo que hace único al sarcoma sinovial.
La Ciencia: Una Cerradura, una Llave y un Soldado Entrenado
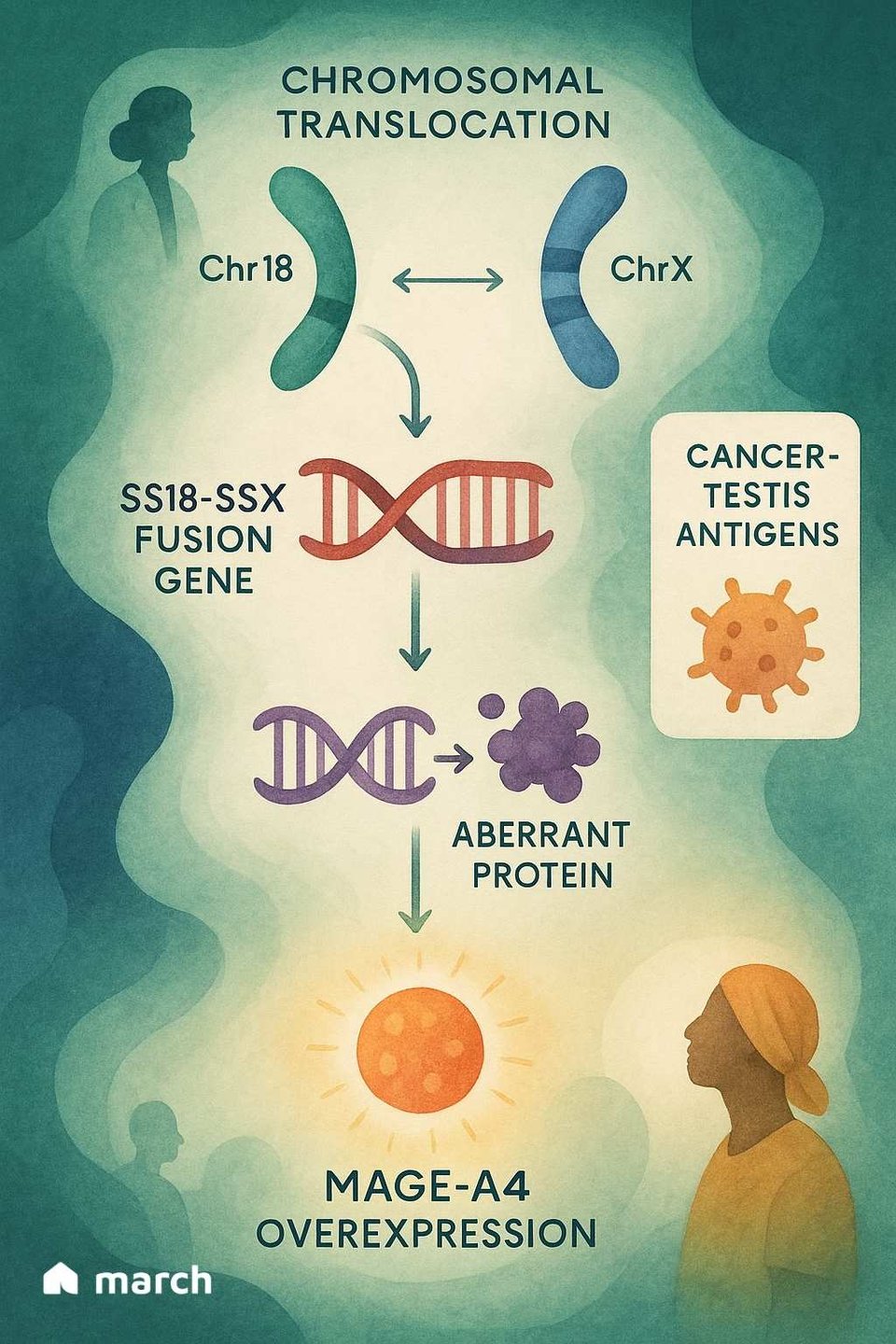
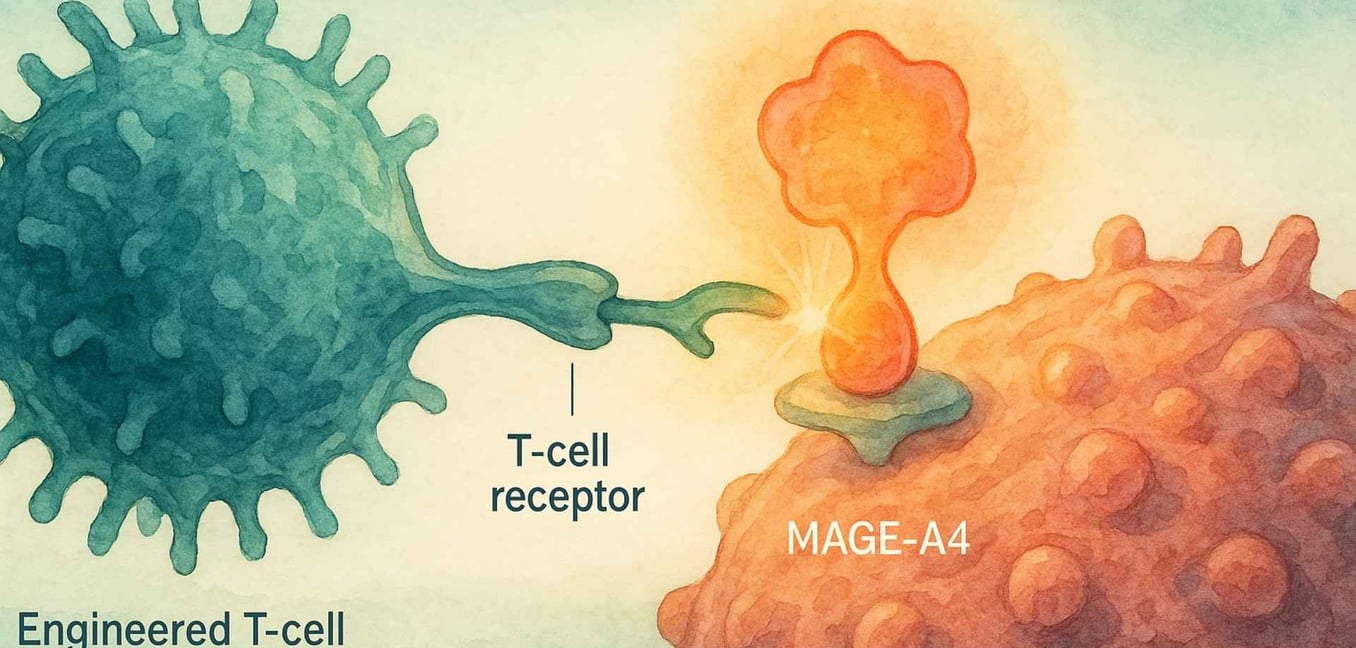
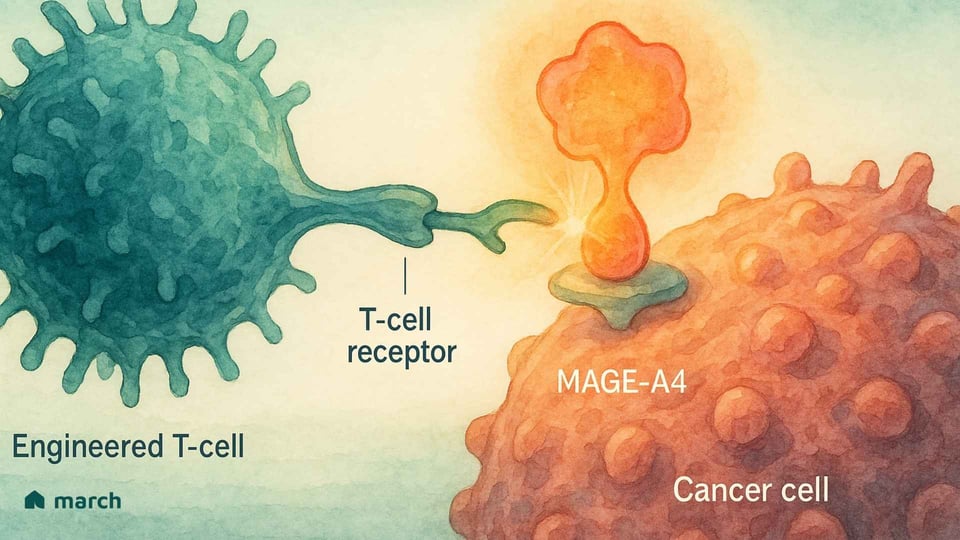
Para comprender verdaderamente la importancia de Tecelra, tenemos que empezar con la biología única del sarcoma sinovial en sí. A diferencia de muchos cánceres que tienen cientos de diferentes mutaciones genéticas, el sarcoma sinovial es a menudo "mutacionalmente silencioso."[4] Más del 95% de los casos son impulsados por un único evento genético específico: una translocación donde partes del cromosoma 18 y del cromosoma X intercambian lugares.[6][7] Esto crea un potente y destructivo gen de fusión llamado SS18-SSX.[6]
Esta proteína de fusión SS18-SSX no causa cáncer por sí misma; en cambio, secuestra la maquinaria interna de la célula que controla qué genes se activan o desactivan.[6] Una de las consecuencias de este caos genético es que las células cancerosas comienzan a producir proteínas que las células adultas normales no producen, incluyendo una proteína llamada MAGE-A4.[8]
MAGE-A4 es un "antígeno cáncer-testículo", lo que significa que normalmente solo se encuentra en sitios privilegiados inmunológicamente como los testículos.[9] Cuando aparece en una célula de sarcoma, actúa como una bandera extranjera, señalando al sistema inmunológico que algo está mal.[8] Aquí es donde entra en juego la elegante estrategia de Tecelra.
De CAR-T a TCR: Apuntando a lo Intocable
Muchos de nosotros hemos oído hablar de la terapia CAR-T, que ha sido revolucionaria para los cánceres de sangre.[10] Las células CAR-T son diseñadas para reconocer objetivos en la superficie de las células cancerosas. Sin embargo, la gran mayoría de las proteínas que conducen el cáncer, como MAGE-A4, están dentro de la célula, haciéndolas invisibles para CAR-T.[20]
Aquí es donde entra la terapia del Receptor de Células T (TCR). Todas nuestras células utilizan un sistema llamado el complejo HLA para mostrar constantemente al sistema inmunológico fragmentos de las proteínas dentro de ellas.[13] Si una célula es cancerosa, mostrará fragmentos de proteínas cancerosas en su superficie. La terapia TCR de células T ingeniería las células T de un paciente para reconocer estos fragmentos muy específicos.[20]
Tecelra es la primera terapia TCR aprobada por la FDA para un tumor sólido, un verdadero logro histórico.[11] Funciona porque resuelve dos problemas a la vez:
La Cerradura (El Objetivo): Le da a las células T de un paciente un nuevo TCR de alta afinidad que está diseñado específicamente para encontrar el fragmento de proteína MAGE-A4.[13]
La Llave (El Apretón de Manos): Solo puede "ver" este fragmento si está siendo presentado por una molécula HLA específica, HLA-A*02.[13]
Este sistema de reconocimiento en dos partes—la "cerradura" MAGE-A4 y la "llave" HLA-A*02—hace que la terapia sea increíblemente precisa, pero también altamente personalizada.[13] Solo funcionará para pacientes que tengan ambos marcadores biológicos.[14]
El Proceso de Tecelra: El Viaje de un Paciente hacia una Medicina Viva
Comprender la ciencia es una cosa; saber lo que realmente implica el viaje es otra. El proceso de recibir Tecelra es intensivo y requiere un compromiso significativo por parte de los pacientes y sus cuidadores. Es un camino de múltiples pasos que transforma las propias células de un paciente en una poderosa medicina viva.
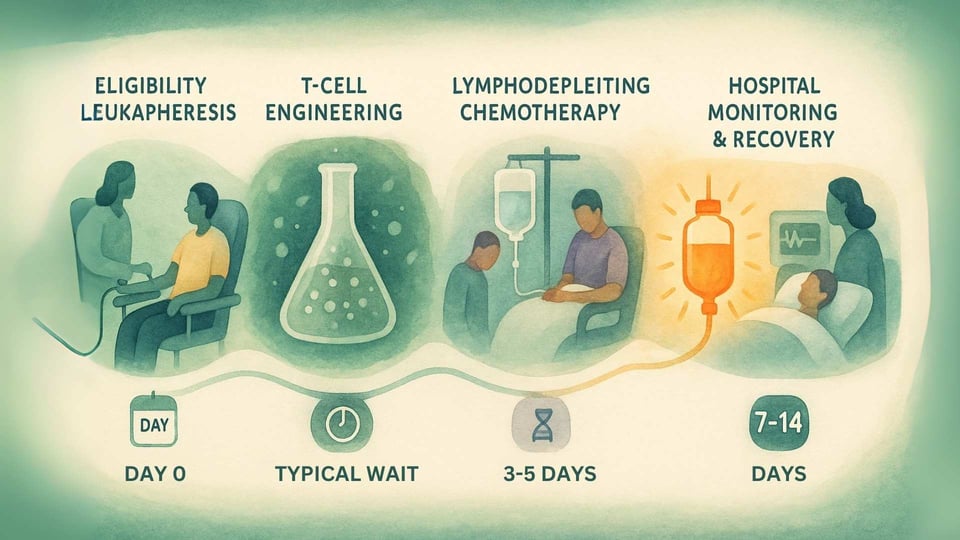
Paso 1: Confirmación y Recolección (Leucaféresis)
El viaje comienza con pruebas para asegurar que un paciente es elegible. Esto implica un análisis de sangre para confirmar que tienen el marcador genético HLA-A*02 requerido y una prueba de biopsia de su tumor para confirmar que expresa la proteína MAGE-A4.[14] Una vez confirmada la elegibilidad, el paciente se somete a leucaféresis, un procedimiento no quirúrgico que filtra las células T de su sangre.[12]
Paso 2: La Espera de Fabricación
Las células T recolectadas se congelan y se envían a una instalación de fabricación especializada. Aquí, pasan por el proceso de ingeniería genética para convertirse en Tecelra.[13] Este es un proceso complejo y cuidadoso que, en el ensayo clínico, tomó una mediana de 40 días.[14] Durante este período de espera, el médico del paciente puede recomendar una "terapia puente", como la quimioterapia, para mantener el cáncer bajo control.[14]
Paso 3: Preparando el Cuerpo (Linfodepleción)
Unos días antes de la infusión, el paciente es ingresado en el hospital para recibir quimioterapia linfodepletora (típicamente fludarabina y ciclofosfamida).[14] El objetivo de esta quimioterapia no es matar el cáncer, sino reducir temporalmente el número de células inmunitarias existentes en el cuerpo.[15] Esto crea un entorno claro y acogedor para que las nuevas células T, diseñadas, se injerten, se expandan y persistan para un efecto duradero.[15]
Paso 4: La Infusión (Día Cero)
Después de la linfodepleción, el paciente recibe sus células Tecelra personalizadas a través de una única infusión intravenosa (IV).[14] Este momento a menudo se llama "Día Cero", marcando el inicio de la lucha de su nuevo sistema inmunológico contra el cáncer.
Paso 5: Monitoreo Intensivo y Apoyo
El período posterior a la infusión es el más crítico. Debido a que la terapia está diseñada para crear una poderosa respuesta inmune, los pacientes deben ser monitoreados en el hospital durante al menos 7 días.[14] También se les aconseja que permanezcan cerca del centro de tratamiento especializado durante al menos 4 semanas. Reconociendo la carga logística y financiera, el fabricante ofrece un programa de apoyo, AdaptimmuneAssist, que puede ayudar a los pacientes elegibles con costos de viaje, alojamiento y otros gastos de bolsillo.[16]
Una Historia Contada en Datos: La Esperanza del Ensayo SPEARHEAD-1
Durante años, esta notable ciencia fue un concepto investigado en laboratorios. Pero el ensayo clínico SPEARHEAD-1 lo trasladó de la teoría a la realidad, ofreciendo esperanza tangible a 44 personas con sarcoma sinovial avanzado que ya habían pasado por una mediana de tres líneas anteriores de terapia sistémica.[14][17] Estos eran pacientes para quienes las opciones estándar habían dejado de funcionar. Los resultados, publicados en la prestigiosa revista The Lancet, fueron una fuente de increíble aliento.[14]
Veamos los números, porque cuentan una poderosa historia de esperanza:
Una Respuesta Significativa (ORR): En este grupo con un tratamiento previo intenso, el 43% de los pacientes vio cómo sus tumores disminuían en respuesta a la infusión única de Tecelra.[11][14] Esto se conoce como la tasa de respuesta general (ORR), y es una cifra significativa donde las terapias en etapas posteriores a menudo tienen tasas de respuesta muy por debajo del 20%.
Beneficios Duraderos y Sostenibles (DoR): Para aquellos que respondieron a la terapia, los efectos a menudo fueron duraderos. La duración mediana de la respuesta (DoR) fue de 6.0 meses.[14] Crucialmente, el 39% de aquellos que respondieron todavía estaban viendo ese beneficio un año después, lo que sugiere un efecto duradero a largo plazo para un grupo significativo.[14]
La "Cola en la Curva" (Supervivencia General): Quizás el hallazgo más poderoso fue lo que les sucedió a los pacientes que respondieron a Tecelra a largo plazo. Para el grupo completo de pacientes con sarcoma sinovial, la supervivencia general mediana (OS) fue de aproximadamente 17 meses.[14] Pero para aquellos cuyo cáncer respondió a la terapia, la OS mediana aún no se había alcanzado, y se estimaba que el 70% de estos respondedores seguían vivos en el punto de dos años.[14] Esto crea lo que los investigadores llaman una "cola en la curva de supervivencia." Sugiere que para un subconjunto de pacientes, esta medicina viva no es solo una solución temporal; tiene el potencial de proporcionar una defensa duradera y a largo plazo contra el cáncer, cambiando fundamentalmente su perspectiva.
Para una comunidad que ha estado esperando más de una década por una nueva opción terapéutica, estos resultados representan un paso monumental y emocional hacia adelante. Es el tipo de progreso que demuestra que la ciencia está escuchando, y que las necesidades de los pacientes con enfermedades raras están impulsando la innovación.
El Camino por Delante: Realismo, Responsabilidad y el Horizonte
Caminamos este camino contigo, sosteniendo tanto la esperanza como la honestidad. Esta es una terapia poderosa, y es crucial entender los efectos secundarios significativos. Debido a que está diseñada para activar poderosamente el sistema inmunológico, Tecelra viene con una Advertencia en la Etiqueta de EE. UU. por dos toxicidades principales, potencialmente mortales:[11]
Síndrome de Liberación de Citoquinas (CRS): Este fue el efecto secundario grave más común, ocurriendo en el 75% de los pacientes en el ensayo.[14] El CRS es una respuesta inflamatoria sistémica que puede causar fiebre alta, náuseas, baja presión arterial y otros síntomas. Mientras que la mayoría de los casos son leves a moderados y pueden ser manejados eficazmente con cuidados de apoyo y medicamentos, el 2% de los pacientes experimentaron CRS severo (Grado 3 o mayor).[14]
Síndrome de Neurotoxicidad Asociado a Células Efectores Inmunes (ICANS): Este es un efecto secundario neurológico más raro, observado en aproximadamente el 2% de los pacientes en un grado bajo.[14]
Estos riesgos son precisamente la razón por la que Tecelra solo puede ser administrado en Centros de Tratamiento Autorizados especializados con equipos entrenados de manera experta.[18]
La llegada de Tecelra es verdaderamente un nuevo amanecer, pero sabemos que no es el final del viaje. La conversación en torno a las terapias avanzadas debe incluir los desafíos de acceso y costo. Con un precio de lista informado de $727,000, garantizar un acceso equitativo es un desafío ético y práctico importante para nuestro sistema de salud.[19] Como defensores, debemos seguir presionando por un futuro en el que cada persona elegible pueda beneficiarse.
La historia de Tecelra es sobre más que solo un solo fármaco. Se trata de la marcha implacable de la ciencia, y abre la puerta a futuras innovaciones. La investigación ya está en marcha explorando otros objetivos, como el antígeno NY-ESO-1 y los TCR de próxima generación diseñados para ser aún más efectivos.[20]
Mientras observamos cómo se desarrolla esta nueva frontera, estamos comprometidos a proporcionarte información clara y confiable. Tus ideas, tus experiencias y tu esperanza son lo que alimenta esta marcha hacia adelante. En este viaje de descubrimiento, no estás solo.
Fuentes
Aytekin, M. N., et al. (2022). El "Gran Disfraz" en Ortopedia: Sarcoma Sinovial. Cureus.
Orphanet. (n.d.). Sarcoma sinovial.
Instituto Nacional del Cáncer. (n.d.). Tratamiento del Sarcoma Sinovial (PDQ®)–Versión para Profesionales de Salud.
King, D.M., et al. (2020). Una revisión del sarcoma sinovial. Journal of the American Academy of Orthopaedic Surgeons.
Martin-Broto, J., et al. (2022). Pazopanib y Trabectedin para Pacientes con Sarcoma Sinovial Metastásico: Un Estudio del Mundo Real. Cancers.
Lagarde, P., et al. (2016). La proteína oncogénica de fusión SS18-SSX. The Journal of Pathology.
PathologyOutlines.com. (n.d.). Sarcoma sinovial - Molecular.
Saito, T., et al. (2023). MAGE-A4 es un posible objetivo terapéutico en el sarcoma sinovial. Oncology Reports.
Instituto de Investigación del Cáncer. (n.d.). Antígenos Cancer-Testis.
Instituto Nacional del Cáncer. (n.d.). Terapia CAR de Células T y sus Efectos Secundarios.
Administración de Alimentos y Medicamentos de EE. UU. (2024). La FDA concede aprobación acelerada a afamitresgene autoleucel.
Instituto Nacional del Cáncer. (n.d.). Leucaféresis. Diccionario de Términos del Cáncer del NCI.
Adaptimmune. (n.d.). Nuestra Tecnología.
D'Angelo, S. P., et al. (2024). Afamitresgene autoleucel para sarcoma sinovial avanzado (SPEARHEAD-1). The Lancet.
Jain, T., et al. (2019). Terapia CAR de Células T: El Papel de la Linfodepleción. The Hematologist.
Adaptimmune. (n.d.). AdaptimmuneAssist.
D'Angelo, S. P., et al. (2021). Afamitresgene autoleucel para sarcoma sinovial avanzado o liposarcoma mixoide/celular redonda. ASCO Post.
Adaptimmune. (n.d.). Centros de Tratamiento Autorizados.
Leo, L. & Sunny, S.E. (2024). La FDA de EE. UU. aprueba la terapia génica de Adaptimmune para el cáncer raro. Reuters.
Ma, S., et al. (2021). Panorama actual de la terapia de células T ingenierizadas con receptores de células T para tumores sólidos. Journal of Hematology & Oncology.