Le Fondement Clair de la Cornée : Le Rôle du Collagène
La cornée humaine est un véritable marvel biologique, agissant à la fois comme un bouclier protecteur robuste pour l'œil interne et comme une fenêtre parfaitement claire pour que la lumière puisse passer. Cette combinaison unique de force et de transparence est principalement due à sa principale protéine structurelle, le collagène. La couche médiane de la cornée, le stroma, représente environ 90 % de son épaisseur totale et est presque entièrement composée de cette protéine vitale. La santé de ce cadre de collagène est directement liée à la capacité de la cornée à fonctionner, et lorsque cela échoue, des conditions débilitantes comme les dystrophies cornéennes peuvent survenir.
L'Architecture d'une Cornée Saine
Pour comprendre ce qui se passe dans la maladie, nous devons d'abord apprécier le design complexe d'une cornée saine. Sa structure est un chef-d'œuvre d'ingénierie biologique, chaque couche jouant un rôle spécifique soutenu par un cadre basé sur le collagène.
La Centrale du Collagène
Le stroma est le principal composant structurel de la cornée. Il se compose de centaines de couches incroyablement fines, ou lamelles, qui sont empilées les unes sur les autres avec une précision remarquable, un peu comme des feuilles de contreplaqué. Chaque lamelle est remplie de fibrilles de collagène de type I parfaitement alignées. Les fibrilles de chaque couche courent dans un angle par rapport à celles des couches au-dessus et au-dessous, créant un arrangement en treillis, semblable à un motif croisé. Ce design est le secret de la force immense de la cornée, tandis que l'espacement uniforme des fibrilles minimise la diffusion de la lumière, garantissant que la vision reste cristalline.
La Barrière Protectrice de la Couche de Bowman
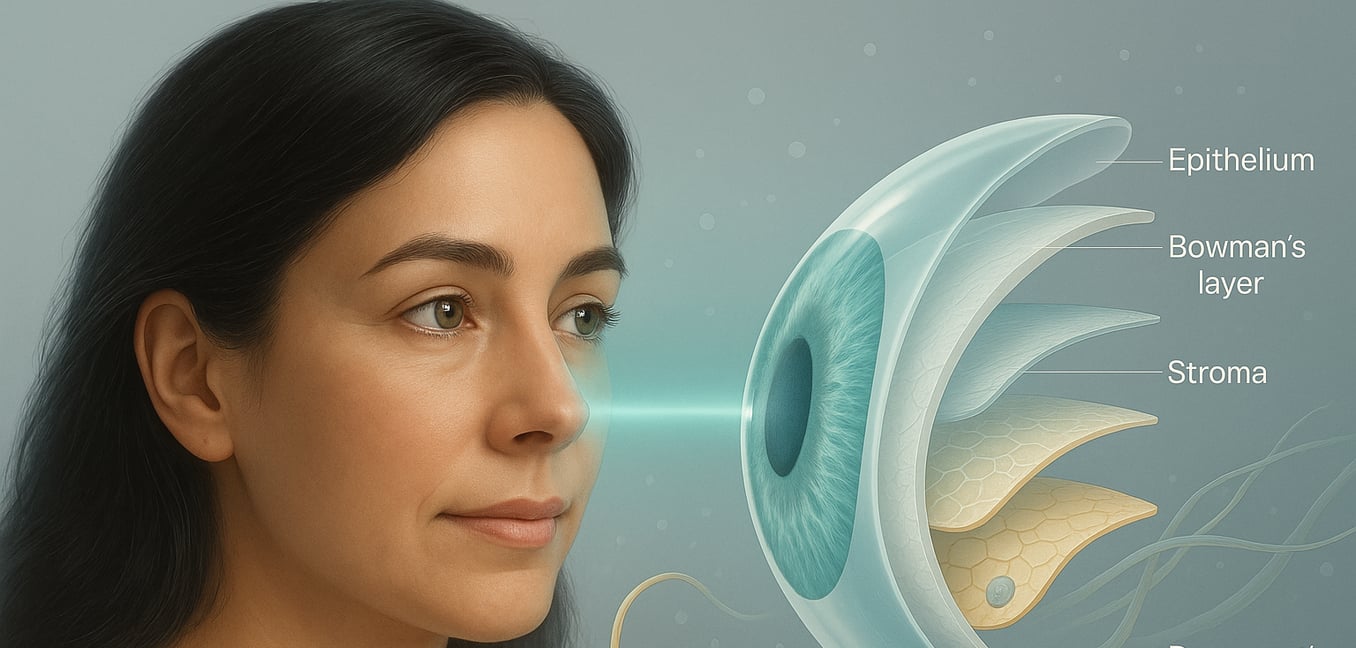
Juste en dessous de l'épithélium de surface de la cornée se trouve la couche de Bowman, une feuille dense et robuste composée de fibrilles de collagène arrangées aléatoirement. Contrairement au stroma hautement organisé, cette couche ne contient aucune cellule et ne peut pas se régénérer si elle est significativement endommagée. Son principal objectif est de servir de barrière protectrice solide, protégeant le stroma sous-jacent des blessures. Elle fournit également une fondation lisse et stable sur laquelle les cellules épithéliales superficielles peuvent s'ancrer et croître, agissant comme une ligne de défense critique pour les structures cornéennes plus profondes.
La Fondamentale Hexagonale de l'Éndothélium
La couche la plus profonde à base de collagène est la membrane de Descemet, qui sert de membrane basale spécialisée pour les cellules endothéliales vitales. Dans une cornée saine, cette membrane n'est pas simplement une feuille simple. Elle possède un motif délicat et cohérent de fines structures hexagonales, créant une échafaudage unique en forme de nid d'abeille. Cette architecture, construite à partir d'une protéine appelée collagène de type VIII, fournit la combinaison parfaite de flexibilité et de soutien pour les cellules endothéliales, leur permettant d'exercer efficacement leur fonction de pompe cruciale.
Dystrophie Cornéenne : Quand le Fondement S'effondre
Lorsque cette intégrité structurelle délicate est compromettue par des facteurs génétiques, un groupe de conditions connues sous le nom de dystrophies cornéennes peut se développer. L'une des plus courantes est la dystrophie endothéliale de Fuchs, une maladie à progression lente qui donne un exemple clair de la manière dont des perturbations dans les couches les plus profondes de la cornée peuvent conduire à une perte de vision significative.
L'Origine de la Perturbation
La caractéristique de la dystrophie de Fuchs est l'apparition progressive de petites excroissances en forme de verrue appelées guttata sur la membrane de Descemet. Ces excroissances ne sont pas des envahisseurs étrangers mais des dépôts anormaux de collagène fibrillaire et d'autres matériaux produits par les cellules endothéliales en détresse elles-mêmes. À mesure que ces dépôts en forme de champignon s'accumulent, ils créent une surface irrégulière souvent décrite comme ayant une apparence de "métal battu" . Cela modifie fondamentalement le fondement structurel sur lequel repose la couche cruciale des cellules endothéliales.
Un Système de Pompe Défaillant
L'endothélium cornéen fonctionne comme une pompe microscopique, éliminant constamment le fluide du stroma pour maintenir la cornée fine et transparente. La formation progressive de guttata étire et finit par détruire ces cellules endothéliales travaillant dur, entraînant une diminution régulière de leur nombre. Bien que les cellules restantes s'agrandissent pour couvrir les espaces, cette solution de bricolage ne peut pas maintenir la puissante fonction de pompe. À mesure que le système échoue, la cornée devient gorgée d'eau, ou œdémateuse. Ce gonflement sépare les fibrilles de collagène soigneusement arrangées dans le stroma, provoquant l'opacité et la vision floue caractéristiques de la maladie.
Un Regard de Plus Près : Comment l'Échec du Collagène Conduit à la Dystrophie de Fuchs
Dans la dystrophie de Fuchs, l'élégante échafaudage hexagonal de collagène de la membrane de Descemet subit une transformation destructrice. Il s'agit d'un processus de remodelage pathologique actif où la cornée crée un fondement entièrement nouveau et dysfonctionnel, qui fait avancer la maladie.
D'abord, la fine structure hexagonale physiologique qui fournit un ancrage flexible pour les cellules endothéliales commence à se décomposer. Ce réseau délicat perd sa cohérence, montrant des zones d'amincissement et de discontinuité. Cette rupture initiale compromet la plateforme stable pour les cellules endothéliales, contribuant à leur stress et à leur éventuelle mort.
En réponse à ce dommage, la cornée initie un processus de réparation défectueux. Elle commence à déposer des faisceaux épais de collagène fibrillaire là où ils n'appartiennent pas. Ce collagène anormal s'organise en un réseau dense, semblable à un nid d'abeille qui s'entrelace autour des guttata, créant une couche épaisse et désorganisée. Ce réseau pathologique n'est pas une restauration de la structure d'origine, mais une réaction cicatricielle qui aggrave davantage la condition.
Ce mur fibreux nouvellement formé crée d'importants problèmes fonctionnels. Sa densité peut contribuer à l'opacité de la cornée et aggraver l'accumulation de fluide, entraînant une plus grande épaisseur cornéenne. Cette barrière cicatricielle est également considérée comme empêchant les cellules endothéliales saines de la périphérie de migrer vers la zone centrale endommagée, entravant toute réparation naturelle.
Le Plan Génétique de la Maladie
Le développement de la dystrophie de Fuchs n'est souvent pas une question de chance ; le plan de la condition se trouve dans le code génétique d'un individu. Pour beaucoup, des mutations spécifiques dans les gènes responsables de la structure cornéenne sont les principaux moteurs, perturbant les processus normaux de maintenance cellulaire et de production de collagène.
Flaws Directes dans les Blocs de Construction
Le gène COL8A2 fournit un lien direct à une forme de dystrophie de Fuchs qui apparaît plus tôt dans la vie. Ce gène détient les instructions spécifiques pour produire un composant du collagène de type VIII, la protéine même qui forme le fondement hexagonal délicat de la membrane de Descemet saine. Lorsque ce plan génétique contient une erreur, le collagène résultant est défectueux. Cela compromet l'architecture de la membrane dès le départ, un exemple classique de la manière dont une anomalie dans un composant structurel peut initier une maladie.
Erreurs dans la Gestion du Site
Le facteur génétique le plus courant pour la dystrophie de Fuchs à début tardif se trouve dans le gène TCF4. Contrairement à COL8A2, qui fournit le plan pour une seule partie, TCF4 agit comme un gestionnaire de chantier. C'est un "facteur de transcription", ce qui signifie qu'il dirige l'activité de nombreux autres gènes impliqués dans la construction et le maintien de la cornée. La mutation la plus courante n'est pas une simple faute de frappe mais un "bégaiement" dans le code génétique - une répétition d'une séquence d'ADN en trois lettres - qui perturbe les instructions du gestionnaire et augmente considérablement le risque de développer la maladie.
Un Tableau Génétique Complexe
L'histoire est encore compliquée par d'autres gènes, tels que SLC4A11 et ZEB1, qui sont responsables de différents travaux cellulaires, du transport d'ions à la spécialisation cellulaire. Cette complexité génétique aide à expliquer pourquoi de nombreux cas ne suivent pas un modèle héréditaire clair et peuvent résulter d'une combinaison de risques génétiques subtils multiples. Cela souligne que la clarté de la cornée dépend d'un large éventail de systèmes parfaitement fonctionnels et interconnectés.