私たちのコミュニティの多くの家族にとって、希少な遺伝病との旅は、体の取扱説明書の中にある一つの小さなエラー—私たちのDNA—から始まります。これらの状態の背後にある科学を理解することが、力を感じるための最初のステップの一つであることを私たちは知っています。数十年間、治療は問題の根本に取り組むのではなく、症状の管理に焦点を当ててきました。しかし、今日、私たちは、これらの状態の核心に迫る素晴らしい科学的進歩の物語を通じて、一緒に歩んでいきたいと思います。
私たちは、「in vivoベース編集」と呼ばれる画期的な技術について、より多くのことを耳にしています。これらの科学用語が intimidating(威圧的)に感じられることを私たちは知っているので、ここでは一緒にそれを分解することを目指しています。これは、私たちのDNAに大きな変化を加えることから、非常に正確な変化を加えることへの物語です。それは、元の遺伝子の誤字を修正するためのより穏やかでターゲットにしたアプローチを提供する「分子鉛筆」の新しい形についてです。[1]
これは、この新しいフロンティアの科学、希望、そして現実的な課題を深く掘り下げるものです。私たちは、これを理解することで、より情報に基づいた会話を持ち、より良い質問をし、未来に何が待っているのかについてより明確な感覚を持って一緒に前進できると信じています。
分子ハサミから遺伝子鉛筆へ:遺伝子編集の進化
ベース編集のブレークスルーを理解するためには、まずそれ以前の技術、すなわちCRISPR-Cas9を見てみることが役立ちます。CRISPRが「分子ハサミ」と表現されているのを聞いたことがあるかもしれません。[1] これは、科学者が私たちのDNAの特定の場所を見つけて切断する能力を与える革命的な発見でした。これは画期的な飛躍で、研究者が不良遺伝子を「オフ」にすることを可能にしました。この技術は、鎌状赤血球病に対して初めて承認されたCRISPRを基盤とした治療、Casgevyの基盤です。細胞は体から取り出され、これらのハサミで編集され、患者に戻されます。
非常に強力である一方、私たちのDNAに二重鎖カットを加えるという考えは常に課題を伴ってきました。その場合、細胞の自然な修復プロセスは少し予測不可能であり、時には意図しない変化を引き起こすことがあります。[2] 体内で広く使用されるためには、どの治療法にも安全性が絶対的な最優先事項です。
ここで、ベース編集が登場します。これは進歩の旅の次のステップを表しています。ハーバード大学とBroad InstituteのDavid Liu博士が率いるチームを含む研究者によって開発されたベース編集は、「分子鉛筆」のようになることを意図して設計されました。[3][4] それは、破壊的なカットを加えることなく、DNAコードの単一の文字に正確な変更を加えるために作成されました。[5][6]
これがどのように機能するかを考えてみましょう:
ガイド:ガイドRNA(gRNA)と呼ばれる分子が、GPS のように機能し、ベースエディターを私たちのDNAを構成する数十億の文字の中の正確で特定の「誤字」に導きます。[1]
アンカー:ベースエディターは、非活性化されたCRISPR蛋白質(しばしばnickaseまたは「死んだ」Cas9と呼ばれる)をアンカーとして使用します。これは、適切な場所でDNAを保持しますが、そしてこれが重要な違いです—二重鎖カットを行いません。[5][7]
鉛筆:このアンカーに結合するのは特別な酵素(脱アミノ化酵素)であり、これが鉛筆として機能します。それは、不正確なDNA文字を効果的に消去し、正しいものに置き換える化学反応を実行します。[7][8]
このアプローチの美しさは、その精度と優しい性質にあります。切断を避けることで、元の「分子ハサミ」に関連する多くの懸念を回避し、希少疾患を引き起こす根本的な遺伝子エラーを修正するための潜在的に安全な方法を提供します。[1][9]
配達の課題:鉛筆を正しいページに届ける
素晴らしい「遺伝子鉛筆」を持つことは一つのことですが、それを体の奥深くにある正しい細胞に届けることは、すべての遺伝子治療における最大の課題の一つです。[2][10] これは「in vivo」というパズルの部分—生体内で編集を行うことです。肝臓、脳、または筋肉など、臓器に影響を与える多くの状態にとって、これは遺伝子治療が機能する唯一の方法です。
科学者たちは、この配達の問題に懸命に取り組んでおり、2つの主要なアプローチが前進しています。それらを2種類の微小な配達トラックとして考えてみてください:
ウイルスベクター(AAVのような):これらは基本的に病気を引き起こさないように空にされ再設計されたウイルスの殻です。代わりに、ベースエディターを作成するための遺伝子指令で満たされています。
利点:ウイルスは自然に細胞に入り込むのが非常に得意であり、さまざまなタイプのアデノ随伴ウイルス(AAV)は、筋肉や目などの特定の組織をターゲットにすることが知られています。[11] 彼らは遺伝子治療研究において長い実績があります。
課題:私たちの体はウイルスと戦うように設計されていることがわかります。これは、治療が行われる前にベクターを阻止する可能性のある既存の免疫を持つ人が多いことを意味します。[12][13] この免疫応答により、二回目の投与が困難になることもあります。[12] さらに、AAVは約4.7キロベースの限られた「貨物スペース」を持っており、これはベース編集機械の収容には窮屈になる可能性があります。[14][15]
脂質ナノ粒子(LNP):あなたはおそらくCOVID-19ワクチンのmRNAに関してこれを聞いたことがあるでしょう。LNPは、ベースエディターのための遺伝子指令(mRNAの形式で)を運ぶことができる小さな脂肪の泡です。[16][17]
利点:LNPはより大きな貨物スペースを持ち、強い免疫応答を引き起こす可能性が低いため、再投与が可能かもしれません。[2][16] 大きな安全上の利点は、彼らが一時的な指令を配達することです。細胞が「鉛筆」を作り、その仕事を終え、その後に指令と鉛筆が自然に排除されます。この短い活動のウィンドウは、望ましくない編集のリスクを減らします。[18]
課題:現在、IVで投与されるとほとんどのLNPは自然に肝臓に取り込まれます。[19][20] これは肝臓疾患の治療には理想的ですが、研究者は体全体の他の組織に向けて指向できる新しいLNPを設計するために熱心に取り組んでいます。[16]
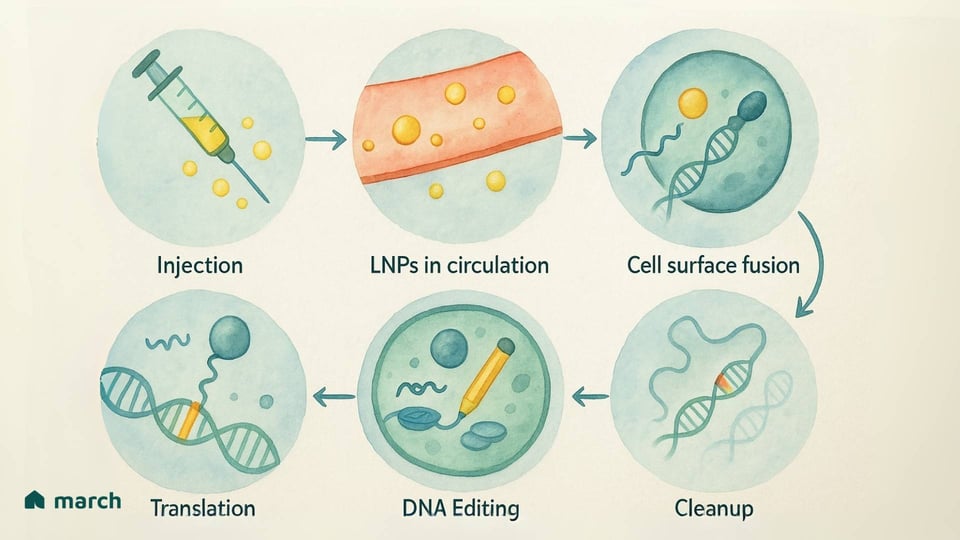
これらの配達システムの進展は、編集ツール自体と同じくらい重要です。これらの「トラック」をより安全でターゲットにしたものにするための一歩前進は、私たちのコミュニティにとって一歩前進です。
画期的な瞬間:in vivoベース編集を受けた最初の人間
この技術は何年もの間、研究室で希望に満ちた研究の対象でした。但し最近、理論から現実に移行する重要な瞬間を目の当たりにしました。深刻で命にかかわる希少 Genetic disease(遺伝病)を抱えて生まれた赤ちゃんK.J. Muldoonの物語は、驚くべきインスピレーションの源です。
K.J.はカルバモイルリン酸合成酵素1(CPS1)欠乏症、肝臓がアンモニアを処理できないという希少な代謝障害を持つと診断されました。これは毒性物質であり、たんぱく質を分解する際に生成される副産物です。[21][22] この状態は壊滅的になりうるもので、推定50%の乳児の死亡率を抱えています。[23] 私たちは、このような診断に伴う恐れと不安を知っています。
しかし、K.J.の特定の状態は、DNAの単一文字の誤字によって引き起こされたものであり—ベース編集の完璧な候補です。驚くべき努力により、彼のために特別に設計されたパーソナライズされた治療法がわずか6か月で作成されました。[21] 彼は、彼の正確な突然変異を修正するために設計されたベースエディタ「鉛筆」のmRNA指示を運ぶLNP—小さな脂肪の泡の静脈内注入を受けました。[24][25]
早期の結果には深い希望が込められています:[23]
K.J.は、彼の食事中のより多くのタンパク質を耐えることができるようになりました。
彼がアンモニアのレベルを制御するために必要な薬の投与量が大幅に削減されました。
彼は発達のマイルストーンに到達し始めました。
最も力強いことに、彼は2つの一般的な子供のウイルスに抵抗し、命にかかわる危機に陥ることなく、克服することができました。このことは、治療される前にはほぼ確実であったことです。
私たちは、この道を希望と現実主義の両方で歩む必要があります。これは一人の勇敢な子供のための治療であり、私たちはまだ修正がどれくらい持続するのかを見る必要があります。[23] しかし、この一つの物語は強力な概念の証明です。この技術が可能であり、生活を変える可能性があることを示しています。また、治療が個々のユニークな遺伝的構造に合わせて調整される未来への扉も開きます。[24]
これはただの一つの物語ではありません。研究は他の条件に対しても活発に進行中です。早老症の実験モデルでは、ベース編集が遺伝子の誤字を修正し、マウスの寿命を劇的に延ばしています。ベース編集を使用した臨床試験も高コレステロールのような状態(Verve Therapeuticsが主導)やα-1アンチトリプシン欠乏症(Beam Therapeuticsが主導)に関して進行中です。[26][27] この研究の波は、多くの異なる患者コミュニティのニーズによって駆動されており、すべての成功が次の成功への勢いを築いています。
共に前進する:今後の旅
in vivoベース編集の夜明けは非常に興奮するものですが、私たちのコミュニティとしては、進展は責任を持って透明性を持って行われなければならないことを知っています。克服すべき重要な課題がまだ残っており、それをオープンに話すことが重要です。
安全性は常に第一:最優先事項は、「鉛筆」が意図したDNA文字のみを編集し、他には何も編集しないことです。科学者たちはこれらの「オフターゲット」編集をチェックするための厳格な方法を開発しており、ツールをさらに正確にするために常に努力しています。[9][28]
長期的な影響を理解すること:永続的な変化を加える治療法については、患者を長期間フォローアップし、利益が持続すること、そして今後思わぬ問題が発生しないことを確認する必要があります。[10][29]
アクセスの課題:これらの高度な治療法が現在非常に複雑で高価であることを私たちは知っています。いくつかの遺伝子治療は、1回の治療で200万ドルを超える費用がかかります。[30][31][32] 私たちのコミュニティとして、私は、これらの人生を変える治療法が、誰がそれらを必要としているかにかかわらず、居住地や資源に関係なく、すべての人にアクセスできる未来を支持することが重要です。[33] これは、最初のうちに、私たちが今行わなければならない会話です。
この分野は静止していません。科学者たちは、DNAの「検索と置換」機能のように機能し、さらに多くのタイプの遺伝子エラー、特に小さな挿入や欠失を修正できる、Dr. Liuのラボからのもう一つの革新であるプライム編集の次世代ツールをすでに開発しています。[34][35][36][37][38][39]
この新しい医療のフロンティアを見守る中で、私たちはあなたに明確で信頼できる情報を提供することを約束します。私たちは、画期的な成果を祝し、課題について正直であり続けます。私たちは、学びあい、共有し、お互いを支援できるコミュニティを築き続けます。あなたの洞察、あなたの経験、そしてあなたの希望は、この前進を促すものです。この発見の旅の中で、あなたは一人ではありません。
簡単な概要については、こちらの新しいポッドキャストエピソードをご覧ください。この治療法の歴史と科学を探ります。
https://youtu.be/-aVHZciahbw
情報源
[7] Menichiello, T. (2023年9月27日). ベース編集とプライム編集:それらが遺伝子治療をどのように変えているか。Cell & Gene.
[30] Rueda, J., de Miguel Beriain, I., & Montoliu, L. (2024). CRISPR治療の手頃な価格は喫緊の倫理的命題である。CRISPR Journal.
[1] BioTechniques. (2017年11月1日). 分子鉛筆が塩基を書き換える。
[40] Verve Therapeutics. (2025). VERVE-102。vervetx.comから取得。
[31] Glick, B. (2023年12月8日). 鎌状赤血球のための高価な遺伝子治療がアクセスのテストを提示します。BioPharma Dive.
[33] CRISPR Therapeutics Canada. (2025年1月28日). CRISPR治療の実際のコスト:カナダの患者が知っておくべきこと。
[8] Genethique. (2017年11月2日). ABE(アデニンベースエディタ):CRISPRツールキットを完成させる「ベースエディタ」。
[21] Technology Networks. (2025年6月27日). 最初のカスタマイズされた遺伝子治療が6ヶ月以内に作成された方法。
[2] Open Access Journals. (n.d.). 遺伝子治療における医師が直面する問題。Journal of Gene Therapy.
[41] Rare Disease Advisor. (2025年4月15日). Verve TherapeuticsがHeFHにおけるPCSK9遺伝子編集に関する有望な結果を報告。
[12] Biocompare. (2025年1月2日). AAVおよびrAAVベースの遺伝子治療の課題を克服する。
[32] Rueda, J., de Miguel Beriain, I., & Montoliu, L. (2024年10月14日). CRISPR治療の手頃な価格は喫緊の倫理的命題である。ResearchGate。
[10] Consensus. (n.d.). 遺伝性疾患の遺伝子治療の開発における課題は何ですか?
[14] Form Bio. (n.d.). 遺伝子治療におけるAAVの役割。
[22] Sanders, R. (2025年5月15日). 致命的な病気を持って生まれた乳児は、出生から6ヶ月後にカスタマイズされたCRISPR治療のおかげで元気になっています。Berkeley News.
[5] Ma, Y., et al. (2023). ベースエディタによる正確なゲノム編集。Journal of Genetics and Genomics.
[34] Howard Hughes Medical Institute. (2020年6月12日). 精密ゲノム編集が現代時代に入る。
[9] MedNexus. (2024). ターゲット遺伝子治療:疾病管理における約束と課題。Journal of Bio-X Research.
[15] BioInnovatise. (2024年12月9日). AAVの包装容量リソース。
[24] Ahn, N. (2025年5月22日). Penn Med, CHOPの研究者がパケットデータの最初の個別遺伝子編集治療を受けた乳児を治療。
[28] Frontiers in Pediatrics. (2024). 小児癌の遺伝子治療戦略における進展と課題:包括的な更新。
[35] Rett Syndrome Research Trust. (n.d.). プライム編集。
[29] Patsnap. (2025年3月20日). 遺伝子治療における倫理的課題は何ですか?
[26] Taylor, N.P. (2025年5月5日). 「より安全な」CRISPR:ベース編集がクリニックで突破口を開く。BioSpace.
[36] Cross, R. (2019年12月2日). CRISPR 3.0の導入。C&EN Global Enterprise.
[23] Garcia de Jesus, E. (2025年5月28日). 個人化された遺伝子編集が赤ちゃんを救ったが、技術の未来は不確かです。Science News.
[37] Synthego. (n.d.). プライム編集:精密遺伝子編集ツールとして。
[6] SCMP. (2023年5月31日). 中国の科学者がCRISPR-Cas9とは異なるアプローチで新しい遺伝子編集ツールを開発。
[27] DeFeudis, N. (2025年3月11日). Beamが肺および肝臓疾患に対する遺伝子編集治療の有望な初期データを共有。Endpoints News.
[42] Wu, G. (2025年3月24日). Verveが米国でのベース編集試験の拡張にFDAの青信号を得た。
[3] Broad Institute. (2025年4月5日). David Liuがライフサイエンスにおけるブレークスループライズを受賞。
[4] Howard Hughes Medical Institute. (2025年4月5日). David Liuがブレークスループライズを受賞。
[43] Rueda, J., de Miguel Beriain, I., & Montoliu, L. (2024). CRISPR治療の手頃な価格は喫緊の倫理的命題である。Digital CSIC.
[13] High, K. A., & Roncarolo, M. G. (2019). AAVベクターへの免疫応答:成功した遺伝子治療への障壁を克服する。Molecular Therapy.
[38] O'Hanlon Cohrt, K. (2023年12月4日). 解説:プライム編集とは何で、何に使用されるのですか?CRISPR Medicine News.
[44] O'Hanlon Cohrt, K. (2025年5月14日). CRISPR Medicine Newsの最新の臨床試験の更新。
[16] GenScript. (2024年10月15日). 脂質ナノ粒子:CRISPR配達システムにおけるブレークスルー。
[39] Davies, H., & Auguste, A. (2023). 精密腫瘍学におけるベースおよびプライムゲノム編集。Cancer Research.
[11] Revvity. (n.d.). AAVベクター:遺伝子治療製造の課題と解決策。
[45] Verve Therapeutics. (2025年5月14日). Verve Therapeutics、パイプラインの進展を発表し、2025年第1四半期の財務結果を報告。
[46] CRISPR Medicine News. (2025年3月11日). Beam Therapeutics、Alpha-1アンチトリプシン欠乏症試験におけるBEAM-302の臨床証明コンセプトデータを報告。
[47] Verve Therapeutics. (2025年4月11日). Verve Therapeutics、PCSK9をターゲットにしたin vivoベース編集医療のための米国FDAのファストトラック指定を取得。
[48] Beam Therapeutics. (2025年3月10日). Beam Therapeutics、α-1アンチトリプシン欠乏症(AATD)における第1/2相試験におけるBEAM-302のポジティブ初期データを発表し、疾病を引き起こす突然変異の臨床的遺伝子修正における初めての臨床試験を実証。
[25] Children's Hospital of Philadelphia. (2025年5月15日). 世界初の患者がフィラデルフィア小児病院で個別のCRISPR遺伝子編集治療を受ける。
[17] ACS Publications. (2022年5月20日). 脂質ナノ粒子を用いたCRISPR/Cas9ゲノム編集コンポーネントの配達。
[18] PubMed Central (PMC). (n.d.). 脂質ナノ粒子:CRISPR-Cas9ゲノム編集におけるゲームチェンジャー。
[49] Promega Connections. (2025年5月28日). ベース編集の輝き:David Liuのブレークスループライズとその影響。
[19] Nano Magazine. (2022年12月19日). 神経細胞ゲノム編集のための脂質ナノ粒子を用いたCRISPRコンポーネントの配達。
[20] ACS Nanoscience Au. (2023年3月30日). mRNA配達のための特定の脂質ナノ粒子における最近の進展。









