私たちのコミュニティの多くにとって、滑膜肉腫との旅は、明確さで始まるのではなく、答えを求めるイライラさせられるしばしば長い探求から始まります。[1] 私たちは、この道がしばしば不確実性に満ちていることを知っています。この癌は稀であり、主に青年や若年成人(AYA人口)に影響を与え、その初期症状は、しばしばゆっくり成長する無痛のしこりであり、スポーツ外傷や嚢腫などのより一般的なものと間違えられがちです。[2][4] これが「診断の冒険」につながり、最大で2年かかる可能性があり、侵襲性の高い癌にとっては致命的な遅延となります。[1]
この診断は、若者たちが人生の重要な時期に直面し、教育、キャリア及び家族計画が中断されます。数十年来、進行または転移性疾患を持つ人々にとっての前進の道は、厳しいものでした。標準的な化学療法レジメは重要ですが、長期的な成功は限られています。[3] 転移性滑膜肉腫と診断された成人の場合、5年総生存率は厳しい10%でした。[3] 第二選択治療として パゾパニブやトラベクトジンは選択肢を提供しますが、典型的には控えめな利点を提供し、中位総生存が約10ヶ月にとどまっています。[5] 真の突破口への非常に深い、切実な未充足のニーズがありました。
しかし今日は、科学的進歩の物語を共に歩み、新たな希望の種類を提供したいと思います。これは癌と戦うだけでなく、患者自身の体にそれを行う方法を教える治療法です。私たちは、「アファミトレスゲン・オートルーセール」またはテセレラについて話しています。[11]
これは科学、希望、そしてこの新たな最前線の現実的な課題への深い洞察です。理解することで、私たちは医療チームとのより情報に基づく会話を持ち、より良い質問をし、未来が何をもたらすかについてのより明確な感覚で共に進むことができると信じています。この治療法は新薬ではなく、新しい章であり、滑膜肉腫を特有なものにする根本に取り組んでいます。
科学:ロック、鍵、訓練された兵士
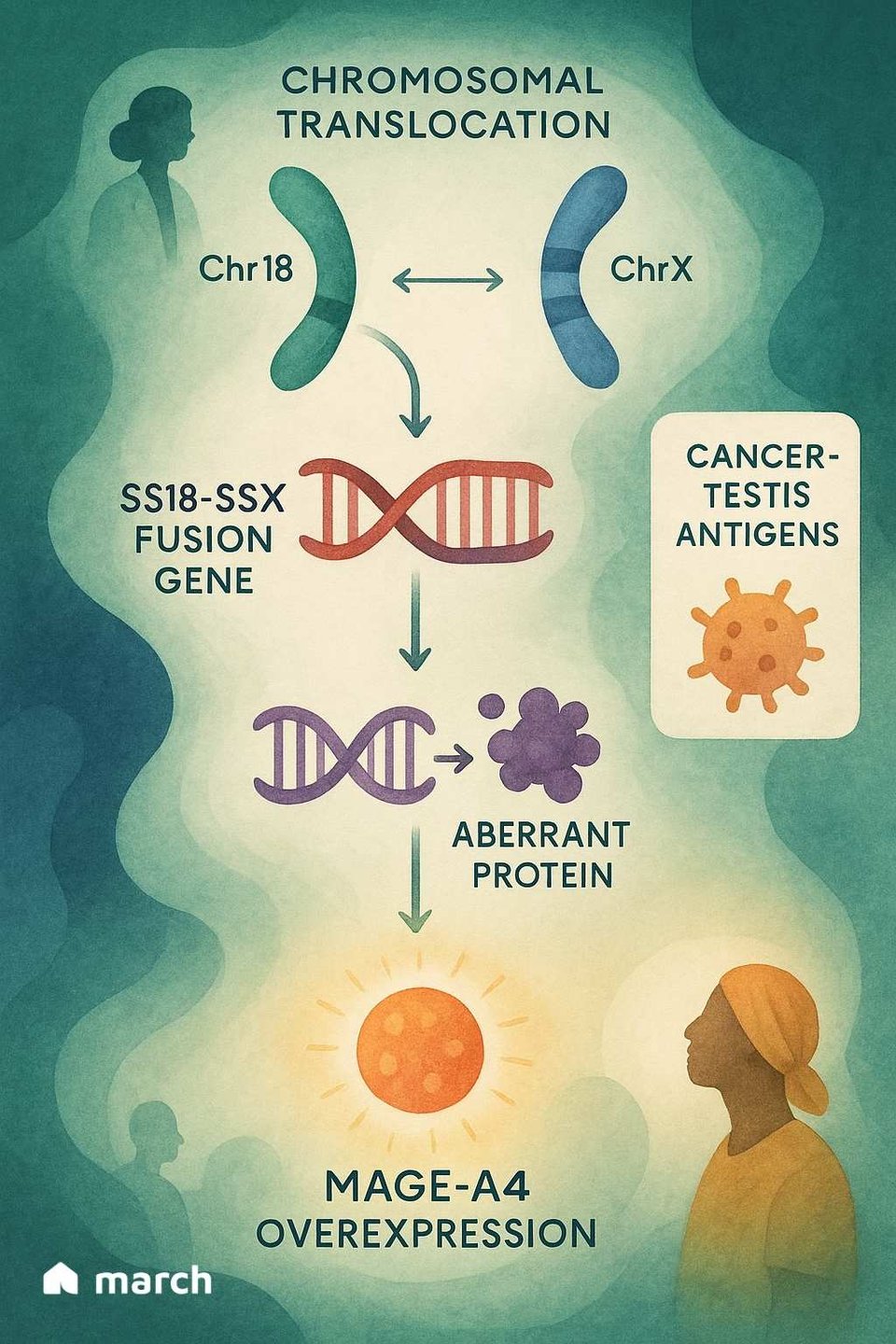
テセレラの重要性を真に理解するためには、滑膜肉腫自身の独特な生物学から始める必要があります。多くの癌は数百の異なる遺伝的変異を持つのとは異なり、滑膜肉腫はしばしば「変異の静穏」です。[4] ケースの95%以上が、染色体18と染色体Xの部分が入れ替わる特定の遺伝的イベントによって引き起こされます。[6][7] これにより、SS18-SSXという強力で破壊的な融合遺伝子が作成されます。[6]
このSS18-SSX融合タンパク質自体が癌を引き起こすわけではありません。むしろ、細胞の内部機構をハイジャックして、どの遺伝子がオンまたはオフになるかを制御します。[6] この遺伝的混乱の結果の1つは、癌細胞が正常な成人細胞が生成しないタンパク質、すなわちMAGE-A4と呼ばれるタンパク質を生成し始めることです。[8]
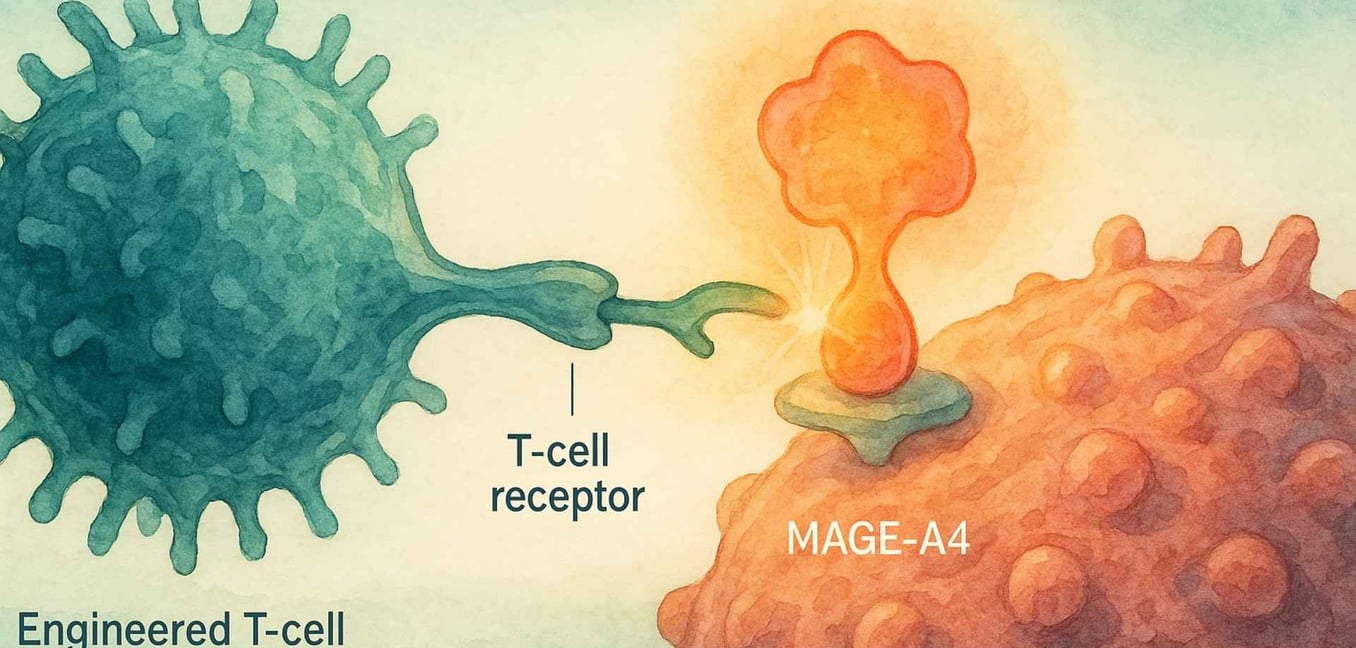
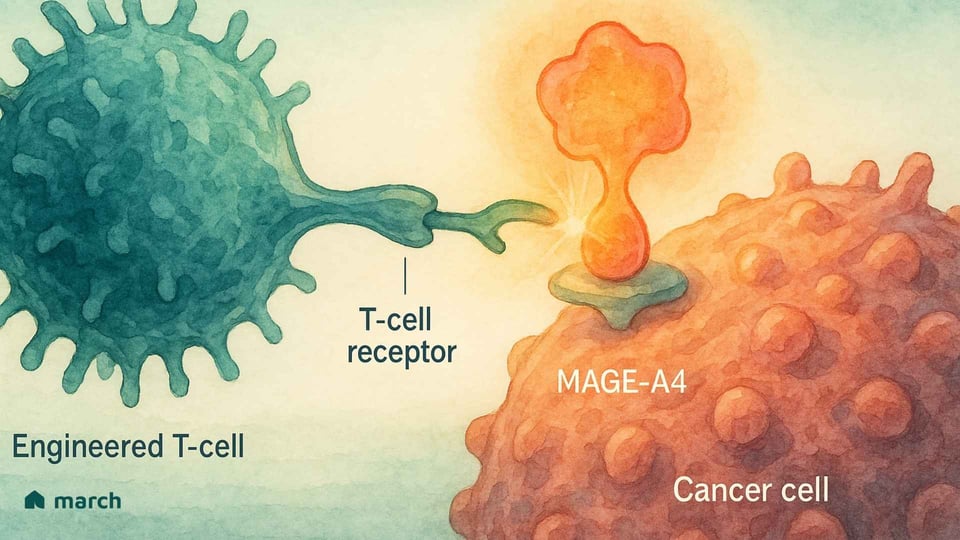
MAGE-A4は「癌-精巣抗原」であり、通常は精巣のような免疫特権の場でのみ見られます。[9] それが肉腫細胞に現れると、それは異物の旗のように振る舞い、免疫系に何かが間違っていることを信号します。[8] ここでテセレラの優雅な戦略が登場します。
CAR-TからTCRへ:手の届かないものをターゲットにする
私たちの多くは、CAR-T療法について聞いたことがあるでしょう。これは血液癌に革命的でした。[10] CAR-T細胞は癌細胞の表面にあるターゲットを認識するように設計されています。ただし、MAGE-A4のような癌を引き起こすタンパク質の大部分は細胞内にあり、CAR-Tからは見えなくなります。[20]
ここで登場するのがT細胞受容体(TCR)療法です。すべての私たちの細胞は、HLA複合体というシステムを利用して免疫系にそれらの内部にあるタンパク質の断片を常に表示します。[13] 細胞が癌性であれば、癌タンパク質の断片をその表面に表示します。TCR T細胞療法は、患者のT細胞がこれらの非常に特定の断片を認識するように設計されています。[20]
テセレラは、固形腫瘍に対してFDAに初めて承認されたTCR療法であり、真の画期的な成果です。[11] それは、2つの問題を同時に解決するから機能します:
ロック(ターゲット):患者のT細胞に、MAGE-A4タンパク質断片を見つけるために巧みに設計された高親和性の新しいTCRを提供します。[13]
鍵(ハンドシェイク):それは特定のHLA分子、HLA-A*02によって提示されている場合にのみこの断片を「見る」ことができます。[13]
この2つの認識システム——MAGE-A4「ロック」とHLA-A*02「鍵」——は、治療法を非常に精密かつ個別化されたものにします。[13] それは、これらの生物学的マーカーの両方を有する患者にのみ機能します。[14]
テセレラプロセス:患者の生きた医薬品への旅
科学を理解することは一つのことですが、実際に何が関わるのかを知ることは別のことです。テセレラを受け取るプロセスは集中的であり、患者とその介護者からの重要なコミットメントを必要とします。これは、患者自身の細胞を強力な生きた医薬品に変換するための多段階の道のりです。
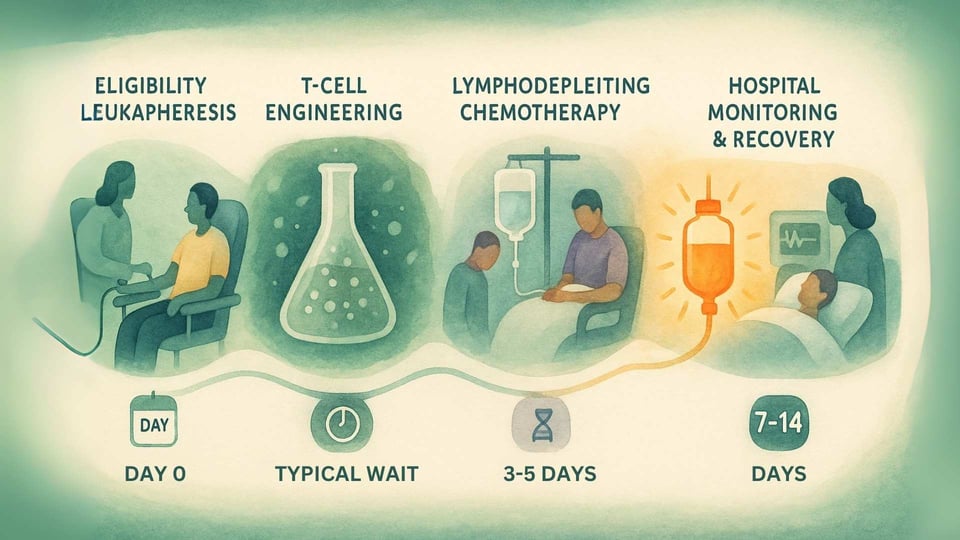
ステップ1:確認と収集(白血球分離)
旅は、患者が適格であることを確認するためのテストから始まります。これには、必要なHLA-A*02遺伝子マーカーを確認するための血液検査と、MAGE-A4タンパク質を表現していることを確認するための腫瘍の生検テストが含まれます。[14] 適格であることが確認されたら、患者は白血球分離を受け、これはT細胞を血液からフィルターする非外科的手順です。[12]
ステップ2:製造待機
収集されたT細胞は凍結され、特別な製造施設に送られます。ここで、テセレラになるための遺伝子工学プロセスを受けます。[13] これは複雑で慎重なプロセスで、臨床試験では中位で40日かかりました。[14] この待機期間中、患者の医者は癌をコントロールするために化学療法などの「ブリッジ療法」を推奨するかもしれません。[14]
ステップ3:身体の準備(リンパ除去)
導入の数日前に、患者は入院し、リンパ除去化学療法(通常はフルダラビンとシクロホスファミド)を受けます。[14] この化学療法の目的は、癌を殺すことではなく、体内の既存の免疫細胞の数を一時的に減少させることです。[15] これにより、新しく設計されたT細胞が移植し、拡大し、長期的な効果を持続させるための明確で快適な環境が作られます。[15]
ステップ4:導入(ゼロ日目)
リンパ除去後、患者は一回の静脈内(IV)導入を通じて個別化されたテセレラ細胞を受け取ります。[14] この瞬間は「ゼロ日目」と呼ばれ、彼らの新しい免疫システムが癌との戦いを始めることを示します。
ステップ5:集中的なモニタリングと支援
導入後の期間は最も重要です。この治療法は強力な免疫反応を作成するために設計されているため、患者は少なくとも7日間病院で監視される必要があります。[14] また、患者は少なくとも4週間専門の治療センターの近くに留まるように勧められます。物流的および財政的な負担を認識し、製造業者は、患者が旅行、宿泊、その他の自己負担費用の支援を受けられるプログラムAdaptimmuneAssistを提供しています。[16]
データで語られた物語:SPEARHEAD-1試験の希望
この注目すべき科学は、何年にもわたって実験室で研究された概念でした。しかし、SPEARHEAD-1臨床試験はそれを理論から現実に移し、すでに中位3回の前治療を受けた進行した滑膜肉腫の44人に具体的な希望を提供しました。[14][17] これらは、標準的なオプションが効かなくなった患者でした。結果は、著名なジャーナルランセットに発表され、驚異的な励ましの源となりました。[14]
数字を見てみましょう。これらは希望の力強い物語を語っています:
意味のある反応(ORR):この治療を強く受けたこのグループでは、43%の患者がテセレラの一回の導入に対して腫瘍が縮小するのを見ました。[11][14] これは全体反応率(ORR)と呼ばれ、後の治療薬では20%を下回ることが多い重要な数字です。
持続的、持続する利益(DoR):治療に応じた患者にとって、その効果は持続することが多かったです。反応の中位持続時間(DoR)は6.0ヶ月でした。[14] 重要なことに、反応した患者の39%は1年後もその利益を実感しており、これは持続的で長期的な効果を示唆しています。[14]
曲線の「尾」(全体生存):おそらく最も強力な発見は、テセレラに反応した患者に何が起こったかです。滑膜肉腫患者全体の中位全生存(OS)は約17ヶ月でした。[14] しかし、治療に反応した患者の場合、中位OSはまだ到達されておらず、これらの反応者の約70%が2年の時点でまだ生存していました。[14] これは研究者が「生存曲線の尾」と呼ぶものを生成します。これは一部の患者にとって、この生きた医薬品が一時的な修正勘ではなく、癌に対しての長期的な持続的防御を提供する可能性を秘めていることを示唆しています。
10年以上にわたって新しい治療の選択肢を待っていたコミュニティにとって、これらの結果は大きな感情的な前進を示しています。これは、科学が耳を傾けており、稀な病の患者のニーズが革新を推進していることを示す進展の類です。
今後の旅路:現実主義、責任、そして地平線
私たちは希望と誠実さを持ってこの道を共に歩みます。これは強力な治療法であり、重大な副作用を理解することが重要です。免疫系を強力に活性化するように設計されているため、テセレラには2つの主な、潜在的に生命を脅かす毒性に対する米国のボックス警告があります:[11]
サイトカイン放出症候群(CRS):これは試験で75%の患者に発生した最も一般的な重篤な副作用でした。[14] CRSは高熱、吐き気、低血圧、およびその他の症状を引き起こす可能性がある全身性の炎症反応です。ほとんどのケースは軽度から中程度で、支持療法や医薬品で効果的に管理できますが、2%の患者が重症(グレード3以上)のCRSを経験しました。[14]
免疫効果細胞関連神経毒性症候群(ICANS):これはまれな神経学的副作用であり、約2%の患者で低い程度で見られました。[14]
これらのリスクは、テセレラが専門の承認治療センターで専門的に訓練されたチームによってのみ投与されることができる理由です。[18]
テセレラの登場は本当に新しい夜明けですが、旅の終わりではないことを私たちは知っています。先進的な治療法に関する会話には、アクセスとコストの課題が含まれる必要があります。報告されたリスト価格が727,000ドルであるため、公平なアクセスを確保することは、私たちの医療システムにとって重要な倫理的かつ実践的な課題です。[19] 擁護者として、私たちはすべての適格な人が利益を受けられる未来を求め続けなくてはなりません。
テセレラの物語は、単なる単一の薬のことではありません。科学の relentless march についてであり、未来の革新への扉を開きます。NY-ESO-1抗原のような他のターゲットの探求や、さらに効果的に設計された次世代TCRの研究がすでに進行中です。[20]
この新しい最前線が展開するのを見守る中で、私たちはあなたに明確で信頼できる情報を提供することに尽力しています。あなたの洞察、あなたの経験、そしてあなたの希望が、この前進を促進する力です。この発見の旅で、あなたは一人ではありません。
出典
Aytekin, M. N., et al. (2022). 整形外科における「偉大な仮面舞踏会」:滑膜肉腫。Cureus。
Orphanet. (n.d.). 滑膜肉腫。
国立癌研究所. (n.d.). 滑膜肉腫治療(PDQ®)–医療専門家版。
King, D.M., et al. (2020). 滑膜肉腫のレビュー。アメリカ整形外科学会誌。
Martin-Broto, J., et al. (2022). 転移性滑膜肉腫の患者におけるパゾパニブとトラベクトジン:実世界の研究。癌。
Lagarde, P., et al. (2016). SS18-SSX融合オンクロプロテイン。病理学ジャーナル。
PathologyOutlines.com. (n.d.). 滑膜肉腫 - 分子。
Saito, T., et al. (2023). MAGE-A4は滑膜肉腫における潜在的な治療ターゲットです。腫瘍学報告。
癌研究所. (n.d.). 癌-精巣抗原。
国立癌研究所. (n.d.). CAR T細胞療法及びその副作用。
米国食品医薬品局. (2024). FDAがアファミトレスゲン・オートルーセールに加速承認を付与。
国立癌研究所. (n.d.). 白血球分離。 NCI癌用語辞典。
Adaptimmune. (n.d.). 我々の技術。
D'Angelo, S. P., et al. (2024). 進行した滑膜肉腫のためのアファミトレスゲン・オートルーセール(SPEARHEAD-1)。ランセット。
Jain, T., et al. (2019). CAR T-細胞療法:リンパ除去の役割。血液学者。
Adaptimmune. (n.d.). AdaptimmuneAssist。
D'Angelo, S. P., et al. (2021). 進行した滑膜肉腫または粘液性/円形細胞脂肪肉腫に対するアファミトレスゲン・オートルーセール。ASCO Post。
Adaptimmune. (n.d.). 承認された治療センター。
Leo, L. & Sunny, S.E. (2024). 米国FDAが稀な癌に対するAdaptimmuneの遺伝子療法を承認。ロイター。
Ma, S., et al. (2021). 固形腫瘍に対するT細胞受容体エンジニアリングT細胞療法の現状。血液学・腫瘍学専門誌。